– простые белки – Биохимия
Структура простых белков представлена только полипептидной цепью (альбумин, инсулин). Однако необходимо понимать, что многие простые белки (например, альбумин) не существуют в “чистом” виде, они всегда связаны с какими-либо небелковыми веществами. Их относят к простым белкам только по той причине, что связи с небелковой группой слабые и при выделении in vitro они оказываются свободным от других молекул – простым белком.
Альбумины
Альбумины – это группа схожих белков плазмы крови с молекулярной массой 69 кДа, содержат много глутаминовой кислоты и поэтому имеют кислые свойства и высокий отрицательный заряд при физиологических рН. Легко адсорбируют полярные и неполярные молекулы, являются белком-транспортером в крови для многих веществ, в первую очередь для билирубина и длинноцепочечных жирных кислот.
В природе альбумины входят в состав не только плазмы крови (сывороточные альбумины), но и яичного белка (овальбумин), молока (лактальбумин), являются запасными белками семян высших растений.
Глобулины
Группа разнообразных белков плазмы крови с молекулярной массой до 100 кДа, слабокислые или нейтральные. Они слабо гидратированы, по сравнению с альбуминами меньше устойчивы в растворе и легче осаждаются, что используется в клинической диагностике в “осадочных” пробах (тимоловая, Вельтмана). Несмотря на то, что их обычно относят к простым, многие глобулины содержат углеводные или иные небелковые компоненты.
При электрофорезе глобулины сыворотки крови разделяются, как минимум, на 4 фракции – α1-глобулины, α2-глобулины, β-глобулины и γ-глобулины.
Картина электрофореграммы (вверху) белков сыворотки крови
и полученной на ее основе протеинограммы (внизу)
Так как глобулины включают в себя разнообразные белки, то их функции разнообразны:
Часть α-глобулинов обладает антипротеазной активностью, что защищает белки крови и межклеточного матрикса от преждевременного разрушения, например, α
1-антитрипсин, α1-антихимотрипсин, α2-макроглобулин.Некоторые глобулины способны к связыванию определенных веществ: трансферрин (переносит ионы железа), церулоплазмин (содержит ионы меди), гаптоглобин (переносчик гемоглобина), гемопексин (транспорт гема).
γ-Глобулины являются антителами и обеспечивают иммунную защиту организма.
Гистоны
Взаимодействие гистонов и ДНК |
Гистоны – внутриядерные белки массой около 24 кДа. Обладают выраженными основными свойствами, поэтому при физиологических значениях рН заряжены положительно и связываются с дезоксирибо-нуклеиновой кислотой (ДНК), образуя дезоксирибо-нуклеопротеины. Существуют 5 типов гистонов – очень богатый лизином (29%) гистон Н1, другие гистоны Н2а, h3b, НЗ, Н4 богаты лизином и аргинином (в сумме до 25%).
Радикалы аминокислот в составе гистонов могут быть метилированы, ацетилированы или фосфорилированы. Это изменяет суммарный заряд и другие свойства белков.
Можно выделить две функции гистонов:
1. Регуляция активности генома, а именно – они препятствуют транскрипции.
2. Структурная – стабилизируют пространственную структуру ДНК.
Гистоны в комплексе с ДНК образуют нуклеосомы – октаэдрические структуры, составленные из гистонов Н2а, h3b, НЗ, Н4. Гистон h2 связан с молекулой ДНК, не позволяя ей “соскользнуть” с гистонового октамера. ДНК обвивает нуклеосому 2,5 раза, после чего обвивает следующую нуклеосому. Благодаря такой укладке достигается уменьшение размеров ДНК в 7 раз.
Далее такие “бусы” нуклеосом могут складываться в суперспираль и в более сложную структуру нуклеопротеина.
Благодаря гистонам и формированию более сложных структур размеры ДНК, в конечном итоге, уменьшаются в тысячи раз: на самом деле длина ДНК достигает 6-9 см (10–1), а размеры хромосом – всего несколько микрометров (10
Протамины
Это белки массой от 4 кДа до 12 кДа, имеются в ядрах сперматозоидов многих организмов, в сперме рыб (молóках) они составляют основную массу белка. Протамины являются заменителями гистонов и служат для организации хроматина в спермиях. По сравнению с гистонами протамины отличаются резко увеличенным содержанием аргинина (до 80%). Также, в отличие от гистонов, протамины обладают только структурной функцией, регулирующей функции у них нет, хроматин в сперматозоидах неактивен.
Коллаген
Коллаген – фибриллярный белок с уникальной структурой, составляет основу межклеточного вещества соединительной ткани сухожилий, кости, хряща, кожи, но имеется, конечно, и в других тканях.
Полипептидная цепь коллагена включает 1000 аминокислот и носит название α-цепь. Насчитывается около 30 вариантов α-цепи коллагена, но все они обладают одним общим признаком – в большей или меньшей степени включают повторяющийся триплет [
Жесткая циклическая структура пролина и оксипролина не позволяет образовать правозакрученную α-спираль, но образует т.н. “пролиновый излом”. Благодаря такому излому формируется левозакрученная спираль, где на один виток приходится 3 аминокислотных остатка.
При синтезе коллагена первостепенное значение имеет гидроксилирование лизина и пролина, включенных в состав первичной цепи, осуществляемое при участии аскорбиновой кислоты. Также коллаген обычно содержит моносахаридные (галактоза) и дисахаридные (глюкоза-галактоза) молекулы, связанные с ОН-группами некоторых остатков оксилизина.
Этапы синтеза молекулы коллагена
Синтезированная молекула коллагена построена из 3 полипептидных цепей, сплетенных между собой в плотный жгут – тропоколлаген (длина 300 нм, диаметр 1,6 нм). Полипептидные цепи прочно связаны между собой через ε-аминогруппы остатков лизина. Тропоколлаген формирует крупные коллагеновые фибриллы диаметром 10-300 нм. Поперечная исчерченность фибриллы обусловлена смещением молекул тропоколлагена друг относительно друга на 1/4 их длины.
Фибриллы коллагена очень прочны, они прочнее стальной проволоки равного сечения. В коже фибриллы образуют нерегулярно сплетенную и очень густую сеть. Например, выделанная кожа представляет собой почти чистый коллаген.
Гидроксилирование пролина осуществляет железо-содержащий фермент пролилгидроксилаза
Гидроксилирование лизина осуществляет фермент лизилгидроксилаза. Она чувствительна к влиянию гомогентизиновой кислоты (метаболит тирозина), при накоплении которой (заболевания алкаптонурия) нарушается синтез коллагена, и развиваются артрозы.
Время полужизни коллагена исчисляется неделями и месяцами. Ключевую роль в его обмене играет коллагеназа, расщепляющая тропоколлаген на 1/4 расстояния с С-конца между глицином и лейцином.
По мере старения организма в тропоколлагене образуется все большее число поперечных связей, что делает фибриллы коллагена в соединительной ткани более жесткими и хрупкими. Это ведет к повышенной ломкости кости и снижению прозрачности роговицы глаза в старческом возрасте.
В результате распада коллагена образуется гидроксипролин. При поражении соединительной ткани (болезнь Пейджета, гиперпаратиреоидизм) экскреция гидроксипролина возрастает и имеет диагностическое значение.
Эластин
Строение десмозина |
По строению в общих чертах эластин схож с коллагеном. Находится в связках, эластичном слое сосудов. Структурной единицей является тропоэластин с молекулярной массой 72 кДа и длиной 800 аминокислотных остатков. В нем гораздо больше лизина, валина, аланина и меньше гидроксипролина. Отсутствие пролина обусловливает наличие спиральных эластичных участков.
Характерной особенностью эластина является наличие своеобразной структуры – десмозина, который своими 4-мя группами объединяет белковые цепи в системы, способные растягиваться во всех направлениях.
α-Аминогруппы и α-карбоксильные группы десмозина включаются в пептидные связи одной или нескольких белковых цепей.
Роль десмозина в соединении белков
Простые белки
Простой белок [1] – это белок, построенный исключительно из остатков ^5,-аминокислот (при гидролизе распадающийся исключительно на аминокислоты [2]), не требующий для функционирования наличия небелковых простетических групп.
Простые белки, по растворимости в солевых растворах и воде, условно подразделяются на несколько групп:
- глобулины,
- альбумины,
- гистоны,
- протамины,
- глютелины,
- проламины.
По пространственному строению и растворимости, простые белки подразделяются на глобулярные и фибриллярные:
- глобулярные простые белки отличаются шарообразной формой молекулы (эллипсоид вращения), хорошо растворяются как в воде, так и в разбавленных солевых растворах. Хорошая растворимость глобулярных белков объясняется локализацией на поверхности глобулы заряженных аминокислотных остатков, окруженных гидратной оболочкой, благодаря чему обеспечивается тесный контакт с растворителем. К глобулярной группе также относятся все ферменты [3] и подавляющее большинство иных биологически активных белков, исключая структурные,
- фибриллярные простые белки характеризуются волокнистой структурой, практически не растворимы как в воде, так и в солевых растворах. Полипептидные цепи [4] в молекулах фибриллярных белков располагаются параллельно одна другой. Данные простые белки принимают участие в образовании структурных элементов соединительной ткани: в эластинах, кератинах, коллагенах.
Белки альбумины и глобулины
Глобулярные простые белки альбумины и глобулины наиболее распространены в растительном и в животном мире, и, как правило, встречаются совместно, составляя основу протоплазмы ( цитоплазмы [5] и ядра клетки [6]).
Наибольшее количество альбуминов и глобулинов содержится в плазме крови [7], тканях организма, сыворотке молока. Альбумины и глобулины в здоровом организме всегда находятся в определенных пропорциях (альбумин – глобулиновый коэффициент [8]).
Альбумины отличаются от глобулинов, как физико-химическими свойствами, так и химическим составом. В частности, альбумины, в отличие от глобулинов, содержат существенно меньшее количество глицина [9] и большее количество серосодержащих аминокислот.
Характерной особенностью белка альбумина является меньшая молекулярная масса в сравнении с глобулинами: молекулярная масса альбумина плазмы крови равна 68000, глобулина – 180000.
Белки глобулины – менее дисперсные и менее гидрофильные (скорее более гидрофобные), чем альбумины, поэтому коллоидные растворы глобулинов не настолько устойчивы, как растворы альбуминов.
Альбумины растворимы в воде в широком диапазоне pH (от 4 pH до 8,5 pH), выпадают в осадок при 70-100% концентрации раствора сульфатом аммония (глобулины – при 50% концентрации). Глобулины сложнее растворяются в воде, при этом растворимы в солевых растворах, обычно содержат углеводную часть.
Белки гистоны и протамины
Глобулярные простые белки гистоны и протамины являются наиболее простыми белками, характерной особенностью которых является слабощелочные свойства растворов. Данный факт обусловлен наличием в составе гистонов и протаминов значительного количества диаминокарбоновых кислот – аргинина [10], лизина [11] и гистидина [12].
Гистоны – низкомолекулярные белки с высоким содержанием в молекуле остатков лизина и аргинина, что обусловливает их основные свойства, содержат 20-35% основных аминокислот, (белки протамины – 50-80%, в связи с чем, протамины проявляют более щелочные свойства, нежели гистоны).
Характерным признаком протаминов является то, они имеют большую молекулярную массу, в сравнении с другими простыми белками. Протамины отличаются еще более высоким содержанием аргинина (до 85 %), и, как и гистоны, образуют устойчивые ассоциаты [13] с нуклеиновыми кислотами [14], выступая в качестве репрессорных и регуляторных белков – составной части нуклеопротеинов.
Гистоны и протамины в значительных количествах содержатся в зобной железе, в икре и сперме рыб, в селезенке. Названия представителей этих простых белков происходят от источника их получения: протамины, выделенные из скумбрии, так и называются – скумбрии, из молоки сельди – клупеином, из молок семги – сальмии.
Гистоны и протамины входят в состав сложных белков в частности нуклеопротеиновых ядер.
Белки глютелины и проламины
Глобулярные простые белки глютелины и проламины – белки растительного происхождения, характеризующиеся высоким содержанием аминокислот пролина и глутаминовой кислоты.
Глютелины на 45 % состоят из глутаминовой кислоты, растворяются в разбавленных кислотах и щелочах, тогда как в воде и разбавленных солевых растворах не растворяются.
Представителями данного класса простых белков является оризенин (белок риса) и глютелин (белок кукурузы).
Глютелины отличаются от проламинов более высоким содержанием гликокола, аргинина, гистидина. По аминокислотному составу белки глютелины сбалансированы лучше, чем белки проламинов.
Проламины, как и глютелины, не растворяются в воде, однако хорошо растворяются в 50-90 % этиловом спирте, состоят на 30-45 % из глутаминовой кислоты и на 15% из пролина.
К проламинам принадлежат глиадин (белок ржи и пшеницы), гордеин (белок ячменя), зеин (белок кукурузы).
Глютелины и проламины составляют подавляющую массу белков зерновых культур.
Белки протеиноиды (склеропротеины)
Фибриллярные простые белки протеиноиды (склеропротеины) – это белки мышечных тканей, кожных покровов, костей, хрящей, волос. Характерной особенностью данных белков является высокая устойчивость к различным растворителям: они не растворяются в воде, растворах нейтральных солей, разбавленных кислотах и щелочах. На протеиноиды не оказывают влияние ферменты, поэтому при попадании в организм с пищей, данные белки крайне плохо усваиваются.
Представителями протеиноидов (склеропротеинов) является эластин, коллаген [15], кератины, фиброин.
Примечания
Примечания и пояснения к статье «Простые белки».
При написании статьи о простых белках, в качестве источников использовались материалы информационных и справочных интернет-порталов, сайтов новостей NCBI.NLM.NIH.gov, ProteinStructures.com, MedicalNewsToday.com, Phys.MSU.ru, IBCh.ru, Википедия, а также следующие печатные издания:
- Гауровиц Ф. «Химия и функции белков». Издательство «Мир», 1965 год, Москва,
- Степанов В. М. «Молекулярная биология. Структура и функции белков. Классический университетский учебник». Издательство «Издательство Московского государственного университета», 2005 год, Москва,
- Ченцов Ю. С. «Введение в клеточную биологию. Классический университетский учебник XXI века». Издательство «Академкнига», 2005 год, Москва,
- Коничев А. С., Севастьянова Г. А. «Молекулярная биология. Высшее профессиональное образование». Издательство «Академия», 2008 год, Москва.
Жми и поделитесь статьей с друзьями:
Характеристика простых белков
В основе классификации (создана в 1908г.) лежит растворимость белков. По этому признаку выделяют:
I. гистоны и протамины, растворимые в солевых растворах. Они относятся к низкомолекулярным белкам (M<5 000 дальтон, Да). В своем составе эти белки содержат большое количество диаминомонокарбоновых кислот (аргинина и лизина). В водной среде они имеют «+» заряд, изоэлектрическая точка (ИЭТ) лежит в области pH 9-12 (щелочная среда).
Основные функции протаминов и гистонов:
1. структурная, т.е. они поддерживают пространственную организацию ДНК и входят в состав ДНП.
2. регуляторная – гистоны регулируют процесс транскрипции.
Протамины имеют меньшую молекулярную массу, чем гистоны; они содержат больше аргинина (до 85%). Происхождение протаминов: сальмин выделен из молок лососевых рыб, скумбрин – скумбрии.
II. Альбумины и глобулины. Это наиболее важные белки плазмы крови (составляют 60%). Содержание альбумина 35-50 г/л, глобулина 20-30 г/л. По форме молекулы это глобулярные белки.
Альбумины растворимы как в воде, так и в солевых растворах, имеют M 40-70 кД (килодальтон, т.е. тысяч дальтон). Особенностью АК-состава является повышенное содержание глутаминовой, аспарагиновой кислот, следовательно в водном растворе эти белки имеют «-» заряд. ИЭТ лежит в пределах pH 4,7 в кислой среде.
В организме альбумины выполняют следующие функции:
1. транспортная – переносят метаболиты, лекарственные вещества, ВЖК (высшие жирные к-ты), холестерины, гормоны, желчные пигменты, ионы Ca2+ и др.
2. поддержание онкотического давления, т.к. осмотическое давление крови на ~75-80% обеспечивается за счет альбуминов.
Глобулины плохо растворимы в воде, но хорошо в солевых растворах. Имеют большую M до 150 кД. Проявляют либо слабовыраженные кислотные, либо нейтральные свойства. ИЭТ лежит в пределах pH 6-7,3.
В норме содержание альбуминов и глобулинов лежит в определенной пропорции – альбумино-глобулиновый или белковый коэффициент: К=А/Г1,5-2,3. Определение АГК имеет диагностическое значение, т.к. при патологиях оно меняется. Например, при инфекционных заболеваниях увеличивается содержание глобулина, АГК уменьшается; при патологии почек нарушается их фильтрационная способность, количество альбуминов уменьшается, следовательно, АГК также падает. Чтобы определить белковый коэффициент необходимо отнести содержание альбумина к содержанию глобулина.
Методы разделения (фракционирования) белков
1. Высаливание – разделение на основе различной растворимости альбуминов и глобулинов. Осаждение белков обычно производят сульфатом аммония (NH4)2SO4. В насыщенном растворе этого реактива осаждаются альбумины, а в полунасыщенном – глобулины.
2. Электрофорез – разделение белков при движении в электрическом поле за счет разности их заряда.
Основные белки сыворотки крови делятся на несколько фракций. Быстрее всех движутся к аноду альбумины – это гомогенная фракция. Глобулины делятся на 4 фракции: 1, 2, , [рис. альбуминов и 4-х глобулинов и как они движутся к аноду].
В крови определяется общий белок. Нормальное общее содержание белка, но изменено соотношение его фракций – диспротенемия. При инфекционных заболеваниях увеличивается содержание g-глобулиновой фракции. При заболеваниях почек снижается содержание альбуминовой фракции, но увеличивается содержание a
III. Проламины и глютелины. Это основные растительные белки. Они не растворяются ни в водных растворах, ни в свободном этаноле, но растворяются в 65% растворе этанола. По АК-составу присутствует глутамин (до 25%), пролин (до 15%). В кукурузе содержится зеин, в ячмене – гордеин, в пшенице – глиадин.
IV. Протеиноиды (склеропротеины). Они не растворяются ни в воде, ни в солевых растворах. Это фибриллярные белки опорных тканей. Входят в состав сухожилий, костной, хрящевой тканей и др. К ним относятся: кератины – белки волос, ногтей; коллагены – белки соединительной ткани; эластины – белки, входящие в состав связок. Особенностью АК-состава является повышенное содержание аланина, глицина, пролина. Имеется оксипролин. Эти белки составляют 25-33% от всех белков в организме.
определение, состав, строение, структура, функции, классификация и характеристика. Чем отличаются простые белки от сложных?
Сложный белок, кроме собственно белкового компонента, содержит дополнительную группу иной природы (простетическую). В качестве данного компонента выступают углеводы, липиды, металлы, остатки фосфорной кислоты, нуклеиновые кислоты. Чем отличаются простые белки от сложных, на какие виды подразделяют эти вещества, и каковы их особенности, расскажет эта статья. Главное отличие рассматриваемых веществ – их состав.
Сложные белки: определение
Это двухкомпонентные вещества, в состав которых входит простой белок (пептидные цепи) и небелковое вещество (простетическая группа). В процессе их гидролиза образуются аминокислоты, небелковая часть и продукты распада. Чем отличаются простые белки от сложных? Первые состоят только из аминокислот.
Классификация и характеристика сложных белков
Эти вещества делятся на виды в зависимости от типа дополнительной группы. К сложным белкам относятся:
- Гликопротеины – белки, молекулы которых содержат углеводный остаток. Среди них выделяют протеогликаны (компоненты межклеточного пространства), включающие в свою структуру мукополисахариды. К гликопротеидам относятся иммуноглобулины.
- Липопротеиды включают липидный компонент. К ним относятся аполипопротеины, выполняющие функцию обеспечения липидного транспорта.
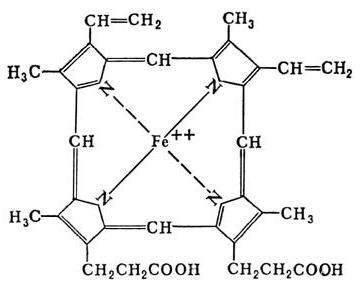
- Металлопротеины содержат ионы металлов (меди, марганца, железа и др.), связанные через донорно-акцепторное взаимодействие. В эту группу не входят гемовые белки, включающие соединения профиринового кольца с железом и подобные им по структуре соединения (хлорофилл, в частности).
- Нуклеопротеиды – белки, имеющие нековалентные связи с нуклеиновыми кислотами (ДНК, РНК). К ним относится хроматин – компонент хромосом.
- 5. Фосфопротеиды, к которым относится казеин (сложный белок творога), включают ковалентно соединенные остатки фосфорной кислоты.
- Хромопротеины объединяет окрашенность простетического компонента. Данный класс включает гемовые белки, хлорофиллы и флавопротеиды.
Особенности гликопротеинов и протеогликанов
Эти белки являются сложными веществами. Протеогликаны содержат большую долю углеводов (80-85%), у обычных гликопротеидов содержание составляет 15-20%. Уроновые кислоты присутствуют только в молекуле протеогликанов, их углеводы отличаются регулярным строением с повторяющимися звеньями. Какова структура и функции сложных белков гликопротеинов? Их углеводные цепи включают только 15 звеньев и имеют нерегулярное строение. В структуре гликопротеинов связь углевода с белковым компонентом обычно осуществляется через остатки таких аминокислот, как серин или аспаргин.

Функции гликопротеинов:
- Входят в состав клеточной стенки бактерий, костной соединительной и хрящевой ткани, окружают волокна коллагена, эластина.
- Играют защитную роль. Например, данную структуру имеют антитела, интерфероны, факторы свертываемости крови (протромбин, фибриноген).
- Являются рецепторами, которые взаимодействуют с эффектором – небольшой небелковой молекулой. Последняя, присоединяясь к белку, приводит к изменению его конформации, что приводит к определенному внутриклеточному ответу.
- Выполняют гормональную функцию. К гликопротеинам относится гонадотропный, адренокортикотропный и тиреотропный гормоны.
- Транспортируют вещества в крови и ионы через клеточную мембрану (трансферрин, транскортин, альбумин, Na+ ,К+ -АТФаза).
К гликопротеиновым ферментам относятся холинэстераза и нуклеаза.
Подробнее о протеогликанах
Обычно сложный белок протеогликан включает в свою структуру большие углеводные цепи с повторяющимися дисахаридными остатками, состоящими из какой-либо уроновой кислоты и аминосахара. Олиго- или полисахаридные цепи называются гликанами. Первые обычно содержат 2-10 мономерных единиц.
В зависимости от структуры углеводных цепей выделяют их различные типы, например, кислые гетерополисахариды с большим количеством кислотных групп или гликозаминогликаны, включающие аминогруппы. К последним относятся:
- Гиалуроновая кислота, которую активно применяют в косметологии.
- Гепарин, препятствующий свертываемости крови.
- Кератансульфаты – компоненты хрящевой ткани и роговицы.
- Хондроитинсульфаты входят в состав хряща и синовиальной жидкости.
Данные полимеры – компоненты протеогликанов, которые заполняют межклеточное пространство, удерживают воду, смазывают подвижные части суставов, являются их структурными составляющими. Гидрофильность (хорошая растворимость в воде) протеогликанов позволяет им в межклеточном пространстве создавать преграду для крупных молекул и микроорганизмов. С их помощью создается желеобразный матрикс, в который погружены волокна других важных белков, например, коллагена. Его тяжи в среде протеогликана имеют древовидную форму.
Особенности и типы липопротеидов
Сложный белок липопротеид отличается хорошо выраженной двойственной гидрофильной и гидрофобной природой. Ядро молекулы (гидрофобную часть) образуют неполярные эфиры холестерола и триацилглицериды.
Снаружи в гидрофильной зоне располагаются белковая часть, фосфолипиды, холестерол. Выделяют несколько разновидностей белков липопротеидов в зависимости от их структуры.
Основные классы липопротеидов:
- Сложный белок высокой плотности (ЛВП, α-липопротеины). Перемещает холестерин к печени и периферическим тканям.
- Низкой плотности (ЛНП, β-липопротеины). Кроме холестерина транспортируют триацилглицериды и фосфолипиды.
- Очень низкой плотности (ЛОНП, пре-β-липопротеины). Выполняют функцию, подобную ЛНП.
- Хиломикроны (ХМ). Транспортируют жирные кислоты и холестерин из кишечника после поступления пищи.
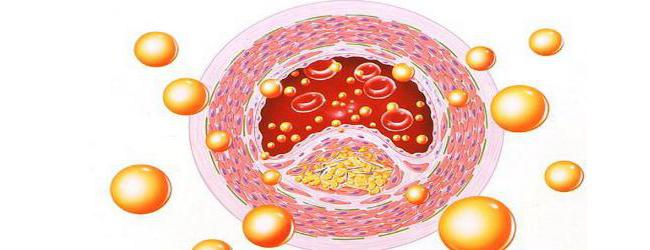
Такая сосудистая патология, как атеросклероз, возникает в результате неправильного соотношения разных типов липопротеинов в крови. По характеристике состава можно выявить несколько тенденций изменения структуры фосфолипидов (от ЛВП до хиломикронов): уменьшение доли белка (от 80 до 10%) и фосфолипидов, увеличение процента триацилглицеридов (от 20 до 90%).
Среди металлопротеинов много важных ферментов
Металлопротеин может включать в себя ионы нескольких металлов. Их наличие влияет на ориентацию субстрата в активном (каталитическом) центре фермента. Ионы металлов локализуются в активном центре и играют важную роль в проведении каталитической реакции. Часто ион выполняет функцию акцептора электронов.
Примеры металлов, содержащихся в структуре ферментных металлопротеинов:
- Медь включена в состав цитохромоксидазы, которая наряду с гемом содержит ион данного металла. Фермент участвует в процессе образования АТФ при работе дыхательной цепи.
- Железо содержат такие ферменты, как ферритин, выполняющий функцию депонирования железа в клетке; трансферрин – переносчик железа в крови; каталаза ответственна за реакцию обезвреживания перекиси водорода.
- Цинк – металл, характерный для алкогольдегидрогеназы, участвующей в окислении этилового и подобных ему спиртов; лактатдегидрогеназа – фермент в метаболизме молочной кислоты; карбоангидраза, катализирующая образование угольной кислоты из CO2 и H2O; щелочная фосфатаза, выполняющая гидролитическое расщепление эфиров фосфорной кислоты с различными соединениями; α2-макроглобулин – антипротеазный кровяной белок.
- Селен входит в состав тиреопероксидазы, участвующей в процессе образования гормонов щитовидной железы; глутатионпероксидазы, выполняющей антиоксидантную функцию.
- Кальций характерен для структуры α-амилазы – фермента гидролитического расщепления крахмала.
Фосфопротеины
Что входит в состав сложных белков фосфопротеинов? Для данной категории характерно присутствие фосфатной группы, которая связана с белковой частью через аминокислоты с гидроксилом (тирозин, серин или треонин). Какие функции выполняет фосфорная кислота, находясь в структуре белка? Она изменяет структуру молекулы, придает ей заряд, повышает растворимость, влияет на свойства белка. Примерами фосфопротеинов являются казеин молока и яичный альбумин, но в основном к данной категории сложных белков относятся ферменты.
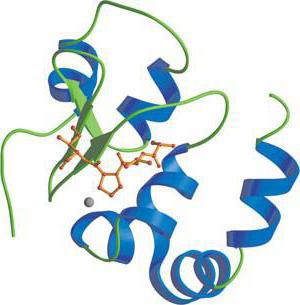
Фосфатная группа играет важную функциональную роль, так как многие белки связаны с ней не постоянно. В клетке все время происходят процессы фосфорилирования и дефосфорилирования. В результате выполняется регуляция в работе белков. Например, если гистоны – белки, соединенные с нуклеиновыми кислотами переходят в фосфорилированное состояние, то активность генома (генетического материала) возрастает. От фосфорилирования зависит активность таких ферментов, как гликогенсинтаза и гликогенфосфорилаза.
Нуклеопротеины
Нуклеопротеины – белки, соединенные с нуклеиновыми кислотами. Они – неотъемлемая часть хранения и регуляции генетического материала, работы рибосом, выполняющих функцию синтеза белка. Самые простейшие формы жизни вирусов можно назвать рибо- и дезоксирибонуклеопротеинами, так как они состоят из генетического материала и белков.
Как происходит взаимодействие дезоксирибонуклеиновой кислоты (ДНК) и гистонов? В хроматине выделяют 2 вида белков, связанных с ДНК (гистоновые и негистоновые). Первые участвуют на начальной стадии компактизации ДНК. Молекула нуклеиновой кислоты обвивается вокруг протеинов с формированием нуклеосом. Образовавшаяся нить похожа на бусины, из них формируются суперспирализованная структура (хроматиновая фибрилла) и суперспираль (хромонема интерфазы). За счет действия гистоновых белков и протеинов более высоких уровней обеспечивается сокращением размерности ДНК в тысячи раз. Достаточно сравнить размер хромосом и длину нуклеиновой кислоты, чтобы оценить важность белков (6-9 см и 10-6 мкм, соответственно).
Какие бывают хромопротеины
Хромопротеины содержат весьма разнообразные группы, которые объединяет только одно – наличие окраски в простетическом компоненте. Сложные белки данной категории подразделяются на: гемопротеины (содержат в структуре гем), ретинальпротеины (витамин А), флавопротеины (витамин В2), кобамидпротеины (витамин В12).
Гемопротеины классифицируются в зависимости от функций на не ферментативные (гемоглобиновый и миоглобиновый белок) и ферменты (цитохромы, каталазы, пероксидазы).
Флавопротеины содержат в качестве простетического компонента производные витамина В2 флавинмононуклеотид (ФМН) или флавинадениндинуклеотид (ФАД). Данные ферменты также участвуют в окислительно-восстановительных превращениях. К ним относятся оксидоредуктазы.
Что такое цитохромы?
Как было описано выше, гем состоит из порфирина. В его структуру входят 4 пиррольных кольца и двухвалентное железо. Особая группа гемовых ферментов – цитохромы, различающиеся составом аминокислот и числом пептидных цепей, специализированы на проведении окислительно-восстановительных реакций, за счет которых обеспечивается перенос электронов в дыхательной цепи. Данные ферменты участвуют в микросомальном окислении – начальных реакциях биотрансформации ксенобиотиков, приводящих к их обезвреживанию, и обмене многих экзогенных и экзогенных веществ, например, стероидов, насыщенных жирных кислот.
Влияние простетической группы
Простетическая группа, входящая в состав сложных белков, влияет на его свойства: изменяет его заряд, растворимость, термопластичность. Например, таким действием обладают остатки фосфорной кислоты или моносахаридов. Углеводная часть, включенная в состав сложного белка, защищает его от протеолиза (разрушения в результате процесса гидролиза), влияет на проникновение молекул через клеточную мембрану, их секрецию и сортировку. Липидный фрагмент позволяет создавать белковые каналы для транспорта плохо растворимых в воде (гидрофобных) соединений.
Строение и функции сложных белков полностью зависят от простетической группы. Например, с помощью железосодержащего гема в гемоглобине происходит связывание кислорода и углекислого газа. За счет нуклеопротеидов, формируемых в результате взаимодействия гистонов, протаминов с ДНК или РНК, происходит защита генетического материала, его компактное хранение, связывание РНК в процессе синтеза белков. Нуклеопротеидами называют устойчивые комплексы белков и нуклеиновых кислот.
Заключение
Таким образом, сложные белки выполняют большой спектр функций в организме. Поэтому потребление макро- и микроэлементов так важно для поддержания здоровья. Металлы входят в состав многих ферментов. Зная биохимию, особенности своего здоровья и экологическое состояние места проживания, можно скорректировать режим собственного питания. Например, выделяют территории, отличающиеся дефицитом какого-либо элемента. Его дополнительное внесение в рацион в виде добавок позволяет восполнить недостаток.
