Белки и их свойства – 2. Классификация и физико-химические свойства белков, строение ферментов. Классификация белков.
2. 1. Общая характеристика белков.
Лекция 2. Химия белков.
Белки – это высокомолекулярные органические, азотсодержащие соединения, состоящие из аминокислот.
Белки – наиболее сложные соединения живых систем. Не только каждый вид живого, но и каждый орган, каждый тип клеток обладает своим специфическим набором белков. Наконец, каждый индивидуум отличается от подобных своего вида собственным набором белков (биохимическая индивидуальность). Эта индивидуальность поддерживается всеми живущими организмами. При внедрении в организм чужих белков образуются защитные вещества (антитела) и разрушают чужие белки. Однако имеется и общность между определенными белками одного и того же вида, которая позволяет проводить обмен белками (например, переливание крови).
В количественном отношении они занимают первое место среди всех содержащихся в живой клетке макромолекул. В организме человека белки составляют примерно 1/5 часть, или 20 % массы, а в пересчете на сухой вес – 45%. Содержание белков в разных тканях различно, так в мышцах и печени содержится до 22 % белка, в мозге – 11 %, в жировой ткани – 6 %.
Свое название белки получили от белого цвета куриного яйца, на примере которого изучались их свойства. В 1838 г. Н. Мульдер назвал белки протеинами (от греч. protos – первый, важный). Это же название принято в международной номенклатуре.
Белки занимают первое место среди макромолекул не случайно, ведь там где есть белки, отмечены признаки жизни и наоборот там где есть жизнь, обнаруживаются белки.
2. 2 Функции белков в организме.
Белки, входящие в состав организма человека, отличаются большим
разнообразием состава, структуры, местом расположения и соответственно функциями.
Белки выполняют следующие функции в организме:
Каталитическая или ферментативная функция. Одна из основных функций белков. В настоящее время известно свыше 2000 различных ферментов, которые являются биологическими катализаторами и ускоряют все биохимические процессы в организме. Практически все они являются по своей химической природе белками.
Структурная или пластическая функция. Еще одна из важнейших функций белков. Мембраны всех клеток и субклеточных единиц представляют собой бислой: белки и фосфолипиды, т.е. белки играют большую роль в формировании всех клеточных структур. Эту функцию выполняют, например следующие белки: кератин – составляет основу волос и ногтей, коллаген – главный белок соединительной ткани.
Сократительная функция. Важным признаком жизни является подвижность, в основе которой лежит данная функция белков, таких как актин и миозин – белки мышц. Кроме мышечных сокращений к этой функции относят и изменение форм клеток и субклеточных частиц.
Транспортная функция. Перенос различных веществ по крови и в пределах клетки. Например, альбумины переносят по крови ВЖК, лекарственные вещества, билирубин; гемоглобин переносит кислород и углекислый газ, другие белки транспортируют липиды, стероиды, витамины и т.д.
Защитная функция. В процессе эволюции в организме выработан механизм узнавания и связывания «чужих» молекул с помощью белков-антител, которые являются белковой фракцией гамма-глобулинов; кроме этого ряд белков, например, альбумины обезвреживают ядовитые вещества (ВЖК и билирубин) в крови; белки свертывающей (фибриноген, протромбин и др.) и противосвертывающей системы предотвращают свертывание крови в нормальных условиях и наоборот образуют сгустки крови при повреждениях сосудов.
- Регуляторная функция. Среди молекул-регуляторов важное место принадлежит регуляторам белковой природы, таким как гормоны, 50% которых имеют белковую природу; белки-гистоны, кислые белки играют роль в регуляции процесса трансляции в биосинтезе белка; белки крови альбумины играют большую роль в создании и поддержании онкотического и осмотического давления крови; белки входя в состав белковой и гемоглобиновой буферных систем участвуют в поддержании рН крови и т.д.
Рецепторная функция. Избирательное связывание различных регуляторов-гормонов, биогенных аминов, простогландинов, медиаторов, циклических мононуклеотидов, протекает с помощью белков-рецепторов на мембранах клетки.
Опорная или механическая функция. Прочность соединительной, хрящевой и костной ткани за счет белков – коллагена, эластина, фибронектина.
Энергетическая функция. 1 г. белка, окисляясь до конечных продуктов – мочевины, углекислого газа и воды, дает 4,1 ккал энергии.
БЕЛКИ: СТРОЕНИЕ, СВОЙСТВА И ФУНКЦИИ
БЕЛКИ: СТРОЕНИЕ, СВОЙСТВА И ФУНКЦИИ
1. Белки и их основные признаки
2. Биологические функции белков
3. Аминокислотный состав белков
4. Классификация белков
5. Физические свойства белков
6. Структурная организация белковых молекул (первичная, вторичная, третичная структуры)
Белки и их основные признаки
Белки или протеины (что в переводе с греческого означает «первые» или «важнейшие»), количественно преобладают над всеми макромолекулами, присутствующими в живой клетке, и составляют более половины сухого веса большинства организмов. Представления о белках как о классе соединений сформировались в XVII-XIX вв. В этот период из разнообразных объектов живого мира (семена и соки растений, мышцы, кровь, молоко) были выделены вещества, обладающие сходными свойствами: они образовывали вязкие растворы, свертывались при нагревании, при горении ощущался запах паленой шерсти и выделялся аммиак. Поскольку все эти свойства ранее были известны для яичного белка, то новый класс соединений назвали белками. После появления в начале XIX вв. Более совершенных методов анализа веществ определили элементный состав белков. В них обнаружили С, Н, О, N, S. К концу XIX вв. Из белков было выделено свыше 10 аминокислот. Исходя из результатов изучения продуктов гидролиза белков, немецкий химик Э.Фишер (1852-1919) предположил, что белки построены из аминокислот.
В результате работ Фишера стало ясно, что белки представляют собой линейные полимеры a-аминокислот, соединенных друг с другом амидной (пептидной) связью, а все многообразие представителей этого класса соединений могло быть объяснено различиями аминокислотного состава и порядка чередования разных аминокислот в цепи полимера.
Первые исследования белков проводились со сложными белковыми смесями, например: с сывороткой крови, яичным белком, экстрактами растительных и животных тканей. Позже были разработаны методы выделения и очистки белков, такие как осаждение, диализ, хроматография на целлюлозных и других гидрофильных ионообменниках, гель-фильтрация, электрофорез. Более подробно рассмотрим эти методы на лабораторной работе и семинарском занятии.
На современном этапе основными направлениями изучения белков являются следующие:
¨ изучение пространственной структуры индивидуальных белков;
¨ изучение биологических функций разных белков;
¨ изучение механизмов функционирования индивидуальных белков (на уровне отдельных атомов, атомных групп молекулы белка).
Все эти этапы взаимосвязаны, ведь одна из основных задач биохимии как раз и состоит в том, чтобы понять, каким образом аминокислотные последовательности разных белков дают им возможность выполнять различные функции.
Биологические функции белков
Ферменты – это биологические катализаторы, самый многообразный, многочисленный класс белков. Почти все химические реакции, в которых участвуют присутствующие в клетке органические биомолекулы, катализируются ферментами. Настоящему времени открыто более 2000 различных ферментов.
Транспортные белки – Транспортные белки плазмы крови связывают и переносят специфические молекулы или ионы из одного органа в другой. Например, гемоглобин, содержащийся в эритроцитах, при прохождении через легкие связывает кислород и доставляет его к периферическим тканям, где кислород освобождается. Плазма крови содержит липопротеины, осуществляющие перенос липидов из печени в другие органы. В клеточных мембранах присутствует еще один клеточный тип транспортных белков, способных связывать определенные молекулы (напр., глюкозу) и переносить их через мембрану внутрь клетки.
Пищевые и запасные белки. Наиболее известными примерами таких белков служат белки семян пшеницы, кукурузы, риса. К пищевым белкам относится яичныйальбумин – основной компонент яичного белка, казеин – главный белок молока.
Сократительные и двигательные белки. Актин и миозин – белки, функционирующие в сократительной системе скелетной мышцы, а также во многих немышечных тканях.
Структурные белки. Коллаген – главный компонент хрящей и сухожилий. Этот белок имеет очень высокую прочность на разрыв. Связки содержат эластин – структурный белок, способный растягиваться в двух измерениях. Волосы, ногти состоят почти исключительно из прочного нерастворимого белка – кератина. Главным компонентом шелковых нитей и паутины служит белок фиброин.
Защитные белки. Иммуноглобулины
или антитела – это специализированные клетки, вырабатываемые в лимфоцитах. Они обладают способностью распознавать проникшие в организм бактерии вирусы или чужеродные молекулы, а затем запускать систему их нейтрализации. Фибриноген и тромбин – белки, участвующие в процессе свертывания крови, они предохраняют организм от потери крови при повреждении сосудистой системы.Регуляторные белки. Некоторые белки участвуют в регуляции клеточной активности. К ним относятся многие гормоны, такие как инсулин (регулирует обмен глюкозы).
Классификация белков
По растворимости
Альбумины. Растворимы в воде и солевых растворах.
Глобулины. Слаборастворимы в воде, но хорошо растворимы в солевых растворах.
Проламины. Растворимы в 70-80% этаноле, нерастворимы в воде и абсолютном спирте. Богаты аргинином.
Склеропротеины. Нерастворимы в воде и солевых растворах. Повышено содержание глицина, аланина, пролина.
По форме молекул
Если исходить из отношения осей (продольной и поперечной), можно выделить два больших класса белков. У глобулярных белков отношение составляет меньше 10 и в большинстве случаев не превышает 3-4. Они характеризуются компактной упаковкой полипептидных цепей. Примеры глобулярных белков: многие ферменты, инсулин, глобулин, белки плазмы крови, гемоглобин.
Фибриллярные белки, у которых отношение осей превышает 10, состоят из пучков полипептидных цепей, спирально навитых друг на друга и связанных между собой поперечными ковалентными или водородными связями (кератин, миозин, коллаген, фибрин).
Физические свойства белков
На физических свойствах белков, таких как ионизация, гидратация, растворимость основаны различные методы выделения и очистки белков.
Так как белки содержат ионогенные, т.е. способные к ионизации аминокислотные остатки (аргинин, лизин, глутаминовая кислота и т.д.), следовательно, они представляют собой полиэлектролиты. При подкислении степень ионизации анионных групп снижается, а катионных – повышается, при подщелачивании наблюдается обратная закономерность. При определенном рН число отрицательно и положительно заряженных частиц становится одинаковым, такое состояние называется изоэлектрическим (суммарный заряд молекулы равен нулю). Значение рН, при котором белок находится в изоэлектрическом состоянии, называют изоэлектрической точкой и обозначают рI. На различной ионизации белков при определенном значении рН основан один из методов их разделения – метод электрофореза.
Полярные группы белков (ионогенные и неионогенные) способны взаимодействовать с водой, гидратироваться. Количество воды, связанное с белком достигает 30-50 г на 100 г белка. Гидрофильных групп больше на поверхности белка. Растворимость зависит от количества гидрофильных групп в белке, от размеров и формы молекул, от величины суммарного заряда. Совокупность всех этих физических свойств белка позволяет использовать метод молекулярных сит или гель-фильтрацию для разделения белков. Метод диализа используется для очистки белков от низкомолекулярных примесей и основан на больших размерах молекул белка.
Растворимость белков зависит и от наличия других растворенных веществ, например, нейтральных солей. При высоких концентрациях нейтральных солей белки выпадают в осадок, причем для осаждения (высаливания) разных белков требуется разная концентрация соли. Это связано с тем, что заряженные молекулы белка адсорбируют ионы противоположного заряда. В результате частицы теряют свои заряды и электростатическое отталкивание, в результате происходит осаждение белка. Методом высаливания можно фракционировать белки.
Первичная структура белков
 |
Первичной структурой белканазывают состав и последовательность аминокислотных остатков в белковой молекуле. Аминокислоты в белке связаны пептидными связями.
Все молекулы данного индивидуального белка идентичны по аминокислотному составу, последовательности аминокислотных остатков и длине полипептидной цепи. Установление последовательности аминокислотной последовательности белков – трудоемкая задача. Более подробно на эту тему мы поговорим на семинаре. Инсулин был первым белком, для которого установили аминокислотную последовательность. Бычий инсулин имеет молярную массу около 5700. Его молекула состоит из двух полипептидных цепей: А-цепи, содержащей 21 а.к., и В-цепи, содержащей 30 а.к., эти две цепи соединены двумя дисульфидными ( -S-S-) связями. Даже небольшие изменения первичной структуры могут значительно изменять свойства белка. Болезнь серповидноклеточная анемия является результатом изменения всего 1 аминокислоты в b-цепи гемоглобина (Glu ® Val).
Видовая специфичность первичной структуры
При изучении аминокислотных последовательностей гомологичных белков, выделенных из разных видов, было сделано несколько важных выводов. К гомологичным белкам относятся те белки, которые у разных видов выполняют одинаковые функции. Примером может служить гемоглобин: у всех позвоночных он осуществляет одну и ту же функцию, связанную с транспортом кислорода. Гомологичные белки разных видов обычно имеют полипептидные цепи одинаковой или почти одинаковой длины. В аминокислотных последовательностях гомологичных белков во многих положениях всегда находятся одни и те же аминокислоты – их называют инвариантными остатками. Вместе с тем в других положениях белков наблюдаются значительные различия: в этих положениях аминокислоты варьируются от вида к виду; такие аминокислотные остатки называютсявариабельными. Всю совокупность сходных черт в аминокислотных последовательностях гомологичных белков объединяют в понятиегомология последовательностей. Наличие такой гомологии предполагает, что животные, из которых были выделены гомологичные белки, имеют общее эволюционное происхождение. Интересным примером является сложный белок – цитохром с – митохондриальный белок, учавствующий в качестве переносчика электронов в процессах биологического окисления. М » 12500, содержит »100 а.к. Были установлены а.к. последовательности для 60 видов. 27 а.к. – одинаковы, это указывает на то, что все эти остатки играют важную роль в определении биологической активности цитохрома с. Второй важный вывод, сделанный на основе анализа аминокислотных последовательностей, состоит в том, что число остатков, по которым различаются цитохромы с любых двух видов, пропорционально филогенетическому различию между данными видами. Например, молекулы цитохрома с лошади и дрожжей различаются по 48 а.к., у утки и курицы – по 2 а.к., у курицы и индейки не различаются. Сведения с числе различий в аминокислотных последовательностях гомологичных белков из разных видов используют для построения эволюционных карт, отражающих последовательные этапы возникновения и развития различных видов животных и растений в процессе эволюции.
Вторичная структура белков
– это укладка белковой молекулы в пространстве без учета влияния боковых заместителей. Выделяют два типа вторичной структуры: a-спираль и b- структуру (складчатый слой). Остановимся более подробно на рассмотрении каждого типа вторичной структуры.
a-Спираль представляет из себя правую спираль с одинаковым шагом, равным 3,6 аминокислотных остатков. a-Спираль стабилизируется внутримолекулярными водородными связями, возникающими между атомами водорода одной пептидной связи и атомами кислорода четвертой по счету пептидной связи.

Боковые заместители расположены перпендикулярно плоскости a-спирали.
 |
Т.о. свойства данного белка определяются свойствами боковых групп аминокислотных остатков: входящих в состав того или иного белка. Если боковые заместители гидрофобны, то и белок, имеющий структуру a-спираль гидрофобен. Примером такого белка является белок кератин, из которого состоят волосы.
В результате получается, что a- спираль пронизана водородными связями и является очень устойчивой структурой. При образовании такой спирали работают две тенденции:
¨ молекула стремится к минимуму энергии, т.е. к образованию наибольшего числа водородных связей;
¨ из-за жесткости пептидной связи сблизиться в пространстве могут лишь первая и четвертая пептидные связи.
В складчатом слое пептидные цепи располагаются параллельно друг другу, образуя фигуру, подобную листу, сложенному гармошкой. Пептидных цепей, взаимодействующих между собой водородными связями, может быть большое количество. Расположены цепи антипараллельно.
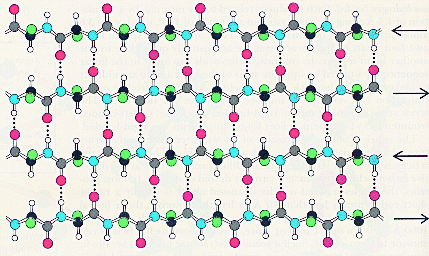 |
Чем больше пептидных цепей входит в состав складчатого слоя, тем прочнее молекула белка.
Сравним свойства белковых материалов шерсти и шелка и объясним различие в свойствах этих материалов с точки зрения строения белков, из которых они состоят.
Кератин – белок шерсти – имеет вторичную структуру a-спираль. Шерстяная нить не такая прочная, как шелковая, легко растягивается в мокром состоянии. Это свойство объясняется тем, что при приложении нагрузки водородные связи рвутся и спираль растягивается.
Фиброин – белок шелка – имеет вторичную b-структуру. Шелковая нить не вытягивается и является очень прочной на разрыв. Это свойство объясняется тем, что в складчатом слое взаимодействуют между собой водородными связями много пептидных цепей, что делает эту структуру очень прочной.
Аминокислоты различаются по способности участвовать в образовании a-спиралей и b-структур. Редко встречаются в a-спиралях глицин, аспаргин, тирозин. Пролин дестабилизирует a-спиральную структуру. Объясните, почему? В состав b-структур входит глицин, почти не встречаются пролин, глютаминовая кислота, аспаргин, гистидин, лизин, серин.
В структуре одного белка могут находиться участки b-структур, a-спиралей и нерегулярные участки. На нерегулярных участках пептидная цепь может сравнительно легко изгибаться, менять конформацию, в то время, как спираль и складчатый слой представляют собой достаточно жесткие структуры. Содержание b-структур и a-спиралей в разных белках неодинаково.
Третичная структура белков
определяется взаимодействием боковых заместителей пептидной цепи. Для фибриллярных белков трудно выделить общие закономерности в образовании третичных структур. Что касается глобулярных белков, то такие закономерности существуют, и мы их рассмотрим. Третичная структура глобулярных белков образуется путем дополнительного складывания пептидной цепи, содержащей b-структуры, a-спирали и нерегулярные участки, так , что гидрофильные боковые группы аминокислотных остатков оказываются на поверхности глобулы, а гидрофобные боковые группы спрятаны вглубь глобулы, иногда образуют гидрофобный карман.
Силы, стабилизирующие третичную структуру белка.
Электростатическое взаимодействие между разно заряженными группами, крайний случай – ионные взаимодействия.
Водородные связи, возникающие между боковыми группами полипептидной цепи.
Гидрофобные взаимодействия.
Ковалентные взаимодействия (образование дисульфидной связи между двумя остатками цистеина с образованием цистина). Образование дисульфидных связей приводит к тому, что удаленные области полипептидной молекулы сближаются и фиксируются. Дисульфидные связи разрушаются под действием восстановителей. Это свойство используется для химической завивки волос, которые почти полностью представляют собой белок кератин, пронизанный дисульфидными связями.
Характер пространственной укладки определяется аминокислотным составом и чередованием аминокислот в полипептидной цепи (первичной структурой). Следовательно, каждый белок имеет только одну пространственную структуру, соответствующую его первичной структуре. Небольшие изменения конформации белковых молекул происходят при взаимодействии с другими молекулами. Эти изменения порой играют огромную роль при функционировании белковых молекул. Так, при присоединении молекулы кислорода к гемоглобину несколько изменяется конформация белка, что приводит к эффекту кооперативного взаимодействия при присоединении остальных трех молекул кислорода. Такое изменение конформации в лежит в основе теории индуцирующего соответствия при объяснении групповой специфичности некоторых ферментов.
Кроме ковалентной дисульфидной все остальные связи, стабилизирующие третичную структуру, являются по своей природе слабыми и легко разрушаются. При разрыве большого числа связей, стабилизирующих пространственную структуру белковой молекулы, упорядоченная уникальная для каждого белка конформация нарушается, при этом часто теряется биологическая активность белка. Такое изменение в пространственном строении называется денатурацией.
Ингибиторы функций белков
Учитывая, что различные лиганды отличаются Ксв, всегда можно подобрать вещество, похожее по структуре на природный лиганд, но имеющий большее значение Ксв с данным белком. Например, СО имеет Ксв в 100 раз больше, чем О2 с гемоглобином, поэтому достаточно 0,1% СО в воздухе, чтобы заблокировать большое количество молекул гемоглобина. По такому же принципу действуют многие лекарства. Например, дитилин.
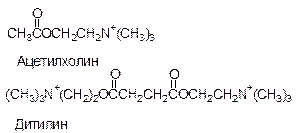
Ацетилхолин – медиатор передачи нервных импульсов на мышцу. Дитилин блокирует белок-рецептор, с которым связывается ацетилхолин и создает эффект парализации.
9.Связь структуры белков с их функциями на примере гемоглобина и миоглобина
Транспорт двуокиси углерода
Гемоглобин не только переносит кислород от легких к периферическим тканям, но и ускоряет транспорт СО2 от тканей к легким. Гемоглобин связывает СО2 сразу после освобождения кислорода (» 15 % всего СО2). В эритроцитах происходит ферментативный процесс образования угольной кислоты из СО2, поступающего из тканей: СО2 + Н2О = Н2СО3. Угольная кислота быстро диссоциирует на НСО3– и Н+. Для предотвращения опасного повышения кислотности должна существовать буферная система, способная поглощать избыток протонов. Гемоглобин связывает два протона на каждые четыре освободившиеся молекулы кислорода и определяет буферную емкость крови. В легких идет обратный процесс. Высвобождающиеся протоны связываются с бикарбонат- ионом с образованием угольной кислоты, которая под действием фермента превращается в СО2 и воду, СО2 выдыхается. Т.о., связывание О2 тесно сопряжено с выдыханием СО2. Это обратимое явление известно как эффект Бора. У миоглобина эффекта Бора не обнаруживается.
Изофункциональные белки
Белок, выполняющий определенную функцию в клетке, может быть представлен несколькими формами – изофункциональными белками, или изоферментами. такие белки хоть и выполняют одинаковую функцию, но отличаются, константой связывания, что приводит к некоторым различиям в функциональном отношении. Например, в эритроцитах человека обнаружено несколько форм гемоглобина: HbA (96%), HbF (2%), HbA2(2%). Все гемоглобины представляют собой тетрамеры, построенные из протомеров a, b, g, d (HbA -a2b2, HbF – a2g2, HbA2 – a2d2). Все протомеры сходны между собой по первичной структуре, и очень большое сходство наблюдается по вторичной и третичной структурам. Все формы гемоглобинов предназначены для переноса кислорода в клетки тканей, но HbF, например, имеет большее сродство к кислороду, чем HbA. HbF характерен для эмбриональной стадии развития человека. Он способен отнимать кислород у HbA, что обеспечивает нормальное снабжение кислородом плода.
Изобелки – это результат наличия более чем одного структурного гена в генофонде вида.
БЕЛКИ: СТРОЕНИЕ, СВОЙСТВА И ФУНКЦИИ
1. Белки и их основные признаки
2. Биологические функции белков
3. Аминокислотный состав белков
4. Классификация белков
5. Физические свойства белков
6. Структурная организация белковых молекул (первичная, вторичная, третичная структуры)
Белки Общая характеристика и функции белков
Белки — важнейшие природные соединения живой клетки как растительной, так и животной.
Основные функции белков в растительном организме те же, что и в животном.
Структурная. Белки участвуют в построении всех клеточных органелл.
Каталитическая. Все ферменты – белки.
Регуляторная. Например, гистоный ряд негистоновых белков регулируют транскрипцию.
Механо-химическая. Белки участвуют в осуществлении движений цитоплазмы и других клеточных органелл.
Транспортная. Белки-переносчики транспортируют различные вещества как через плазматическую мембрану, так и внутри клетки.
Защитная. Например, гидролитические ферменты лизосом и вакуолей расщепляют вредные вещества, попавшие в клетку. Кроме того, гликопротеины участвуют в защите растений от патогенов.
Запасная. Эта функция характерна в основном для растений. Запасные белки откладываются в семенах и используются для питания проростков в процессе прорастания.
В настоящее время функции многих белков еще не выяснены. Кроме того, один белок может выполнять две или более функций. Например, некоторые белки мембран могут выполнять структурную и ферментативную функции.
Как правило, содержание белков в растениях ниже, чем у животных. В вегетативных органах количество белка обычно 5-15% от сухой массы. Так, в листьях тимофеевки содержится 7% белка, а в листьях клевера и вики — 15%. Больше белка в семенах: у злаков в среднем 10-20%, у бобовых и масличных — 25-35%.
Наиболее богаты белком семена сои — до 40%, а иногда и выше. В растительных клетках белки обычно связаны с углеводами, липидами и другими соединениями, а также с мембранами. Поэтому их трудно извлекать из растений и получать чистые препараты, особенно из вегетативных органов. В связи с этим в растениях лучше изучены белки семян, где их больше и откуда они легче извлекаются.
Растительные белки по своим свойствам, молекулярной массе и структуре молекул близки к белкам животного происхождения.
Мономерами белков являются аминокислоты. В составе белков как растительных, так и животных, найдено 20 аминокислот:
В растениях, кроме 20 перечисленных выше, обнаружено большое количество аминокислот (свыше 250), которые не входят в состав белковых молекул, а содержатся только в свободном состоянии или встречаются в составе коротких пептидов. Их называют не протеиногенными. Эти аминокислоты присутствуют в растениях в небольших количествах и обычно характерны для небольшой группы растений (семейство, род).
Пептиды, или полипептиды,— это цепочки из нескольких аминокислот, связанных пептидными связями. В состав пептидов могут входить не только протеиногенные, но и непротеиногенные аминокислоты.
Пептиды играют важную роль промежуточных продуктов в обмене веществ, и многие из них являются физиологически очень активными соединениями. Пептидами являются некоторые антибиотики (грамицидин, лихениформин), гормоны (инсулин, окситацин, вазопрессин), токсины (аманитины). Некоторые пептиды представляют собой замкнутую полипептидную цепочку, т. е. являются циклопептидами, а некоторые даже имеют бициклическое строение. Среди циклопептидов есть сильно токсичные вещества. Например, ядовитый гриб бледная поганка (Amanita phalloides) содержит по крайней мере 10 токсичных циклопептидов — аманитинов. Все они имеют молекулярную массу около 1000.
2. Классификация и физико-химические свойства белков, строение ферментов. Классификация белков.
Классификация белков базируется на их химическом составе. Согласно этой классификации белки бывают простые и сложные. Простые белки состоят только из аминокислот, то есть из одного или нескольких полипептидов. К простым белкам, имеющимся в организме человека, относятся альбумины, глобулины, гистоны, белки опорных тканей.
В молекуле сложного белка, кроме аминокислот, ещё имеется неаминокислотная часть, называемая простетической группой. В зависимости от строения этой группы выделяют такие сложные белки, как фосфопротеиды(содержат фосфорную кислоту), нуклеопротеиды( содержат нуклеиновую кислоту), гликопротеиды(содержат углевод), липопротеиды(содержат липоид) и другие.
Согласно классификации, которая базируется на пространственной форме белков, белки разделяются на фибриллярные и глобулярные.
Фибриллярные белки состоят из спиралей, то есть преимущественно из вторичной структуры. Молекулы глобулярных белков имеют шаровидную и эллипсоидную форму.
Примером фибриллярных белков является коллаген – самый распространенный белок в теле человека. На долю этого белка приходится 25-30% от общего числа белков организма. Коллаген обладает высокой прочностью и эластичностью. Он входит в состав сосудов мышц, сухожилий, хрящей, костей, стенки сосудов.
Примером глобулярных белков являются альбумины и глобулины плазмы крови.
Физико-химические свойства белков.
Одной из главных особенностей белков является их большая молекулярная масса, которая колеблется в диапазоне от 6000 до нескольких миллионов дальтон.
Другим важным физико-химическим свойством белков является их амфотерность, то есть наличие, как кислотных, так и основных свойств. Амфотерность связана с наличием в составе некоторых аминокислот свободных карбоксильных групп, то есть кислотных, и аминогрупп, то есть щелочных. Это приводит к тому, что в кислой среде белки проявляют щелочные свойства, а в щелочной среде – кислотные. Однако при определенных условиях белки проявляют нейтральные свойства. Значение рН, при котором белки проявляют нейтральные свойства, называется изоэлектрической точкой. Изоэлектрическая точка для каждого белка индивидуальна. Белки по этому показателю делят на два больших класса – кислые и щелочные, так как изоэлектрическая точка может быть сдвинута либо в одну, либо в другую сторону.
Еще одно важное свойство белковых молекул – это растворимость. Несмотря на большой размер молекул белки довольно хорошо растворимы в воде. Причем растворы белков в воде весьма устойчивы. Первой причиной растворимости белков является наличие на поверхности молекул белков заряда, благодаря чему белковые молекулы практически не образуют нерастворимые в воде агрегаты. Второй причиной устойчивости белковых растворов является наличие у белковой молекулы гидратной (водной) оболочки. Гидратная оболочка отделяет белки друг от друга.
Третье важное физико-химическое свойство белков – это высаливание, то есть способность выпадать в осадок под действием водоотнимающих средств. Высаливание – процесс обратимый. Эта способность то переходить в раствор, то выходить из него очень важна для проявления многих жизненных свойств.
Наконец, важнейшим свойством белков является его способность к денатурации. Денатурация – это потеря белком нативности. Когда мы делаем яичницу на сковороде, мы получаем необратимую денатурацию белка. Денатурация заключается в постоянном или временном нарушении вторичной и третичной структуры белка., но при этом первичная структура сохраняется. Помимо температуры(выше 50 градусов) денатурацию могут вызвать другие физические факторы: излучении, ультразвук, вибрация, сильные кислоты и щелочи. Денатурация может быть обратимой и необратимой. При небольших воздействиях разрушение вторичной и третичной структур белка происходит незначительное. Поэтому белок при отсутствии денатурирующего воздействия может восстановить свою нативную структуру. Процесс обратный денатурации называется ренатурация. Однако при продолжительном и сильном воздействии ренатурация становится невозможной, а денатурация, таким образом, необратимой.
Белок-белковые взаимодействия — Википедия
 Белок-белковое взаимодействие подковообразного ингибитора рибонуклеазы (показана каркасная модель) с рибонуклеазой. Контакты между двумя белками показаны цветными пятнами
Белок-белковое взаимодействие подковообразного ингибитора рибонуклеазы (показана каркасная модель) с рибонуклеазой. Контакты между двумя белками показаны цветными пятнамиБелок-белковые взаимодействия (ББВ) — обладающие высокой специфичностью физические контакты между двумя и более белками. Эти контакты образуются в результате биохимических событий с помощью электростатических взаимодействий, в том числе гидрофобного эффекта[en][1].
Белки — важные макромолекулы как для внутриклеточных, так и для внешних процессов. Белки редко действуют в одиночку: для участия в различных жизненно важных процессах внутри клетки эти макромолекулы с помощью белок-белковых взаимодействий собираются в мультибелковые комплексы. Белок-белковые взаимодействия составляют основу интерактома любой живой клетки[1]. Они участвуют в таких важных клеточных процессах, как передача сигнала, клеточное общение, транскрипция, репликация, мембранный транспорт и другие. Поэтому неудивительно, что нарушения этих взаимодействий приводят ко многим заболеваниям, таким как болезнь Крейтцфельдта — Якоба, болезнь Альцгеймера и рак[2].
Не все белок-белковые взаимодействия образуются раз и навсегда. Часть белков входит в состав стабильных комплексов, которые являются молекулярными машинами (например, АТФ-синтаза или цитохромоксидаза). Другие же белки собираются обратимо для осуществления какой-либо временной функции (например, для активации экспрессии генов в случае с транскрипционными факторами и активаторами)[1].
Белок-белковые взаимодействия рассматриваются со стороны биохимии, квантовой химии, молекулярной динамики, передачи сигналов в клетке[3]. Полученная информация позволяет создавать обширные сети белковых взаимодействий, похожих на метаболические или генетические/эпигенетические связи. Это расширяет текущие знания о биохимических каскадах и патогенезе заболеваний, а также открывает новые возможности для поиска новых терапевтических мишеней.
Белки могут «временно» связываться друг с другом или же образовывать «стабильные» мультибелковые комплексы. При этом белковые комплексы могут быть как гетеро-, так и гомоолигомерными. Классическими примерами ББВ являются взаимодействия фермент-ингибитор и антитело-антиген, но помимо них ББВ могут возникать между двумя доменами или же доменом и пептидом[1].
Гомо- и гетероолигомеры[править | править код]
Гомоолигомеры — макромолекулярные комплексы, состоящие только из одного типа белковых субъединиц. Если же связь образуется между неидентичными белковыми цепями, то образуется гетероолигомер. Гетероолигомеры разнятся по своей стабильности, а для большинства гомоолигомерных комплексов характерна симметричность и стабильность. Разборка гомоолигомеров зачастую требует денатурации[4]. Некоторые ферменты, транспортные белки, факторы транскрипции выполняют свою функцию будучи гомоолигомерами. Взаимодействия между разными белками играют большую роль в клеточной передаче сигналов.
Обязательные и необязательные взаимодействия[править | править код]
Для разделения ББВ на обязательные и необязательные нужна информация о стабильности участвующих во взаимодействии белков (мономеров) в свободном состоянии и в составе белкового комплекса. Если мономеры стабильны in vivo только в составе комплекса, то взаимодействие между ними является обязательным. В результате обязательных взаимодействий формируются обязательные или облигатные комплексы. Если же белки могут существовать независимо, то они участвуют в необязательных ББВ. Большинство макромолекулярных машин в клетке являются примерами обязательных взаимодействий[2]. К обязательным комплексам относятся человеческий катепсин D и димер ДНК связывающего белка P22 Arc repressor, а необязательных взаимодействий — взаимодействие RhoA с RhoGAP и тромбина со своим ингибитором родниином[5].
Постоянные и временные взаимодействия[править | править код]
ББВ можно разделить по времени жизни комплекса. Постоянные взаимодействия обычно очень стабильны: белки, взаимодействуя, образуют постоянныей комплекс. Они часто присутствуют в гомоолигомерах (например, Цитохром с) и в некоторых гетероолигомерах (например, субъединицы АТРазы). Временные взаимодействия постоянно образуются и разрушаются. Они могут возникать при взаимодействии гормона с рецептором, передаче клеточного сигнала. Такой тип взаимодействия широко распространён в сигнальных и регуляторных путях[2].
Ковалентные и нековалентные взаимодействия[править | править код]
Ковалентные связи — наиболее прочные и образуются в случае обмена электронами (например, дисульфидные связи). Хотя эти связи редко встречаются при белок-белковых взаимодействиях, в некоторых посттрансляционных модификациях они являются определяющими (например, убиквитирование и навешивание SUMO белков). Нековалентные связи обычно образуются во временных взаимодействиях за счет комбинаций слабых связей: водородных, ионных, ван-дер-ваальсовых или гидрофобных[6].
Переход из неструктурированного в структурированное состояние[править | править код]
Отдельно можно выделить ББВ, которые образуются частично неструктурированными белками[en]. В таких белках есть участки, аминокислотная последовательность которых не позволяет образовать стабильной третичной структуры. Эти белки могут взаимодействать с другими, подбирая подходящую конформацию для образования связи с партнёром[2].
Трёхмерная структура белковых комплексов[править | править код]
Молекулярные структуры многих белковых комплексов были разрешены с помощью рентгеноструктурного анализа[7][8]. Первой такой структурой был миоглобин кашалота[9]. Позднее для определения трёхмерной структуры белковых комплексов также стали применять ЯМР. Так, например, одной из первых была получена структура кальмодулин-связанных доменов, взаимодействующих с кальмодулином[8][10]. Этот метод хорошо подходит для определения слабых белок-белковых взаимодействий[11].
Домены[править | править код]
Благодаря развитию методов разрешения трёхмерной структуры белков удалось выделить структурные домены, которые участвуют в образовании ББВ. Такими, например, являются:
- Sh3-домен, связывающий фосфорилированные белки;
- Sh4-домен, специфичный к пролин-богатым последовательностям;
- PTB-домен, взаимодействующий с последовательностями, содержащими фосфотирозиновую группу;
- LIM-домен, содержащий цистеин-богатый мотив цинкового пальца и способный связываться с PDZ-доменом и себе подобными;
- SAM-домен, связывающий белки, не содержащие данный домен;
- PDZ-домен, узнающий мотив S/TXV на C-конце белка, а также LIM-домены или себе подобные;
- FERM-домен, способный связывать PI(4,5)P2 (фосфоинозитол-4,5-бисфосфат)[12].
Биологические эффекты белок-белковых взаимодействий[править | править код]
Белок-белковые взаимодействия играют важную роль во многих биологических процессах. Функция и активность белка в большинстве случаев изменяются при связывании с белками-партнёрами. Они могут оказывать значительное влияние на кинетические параметры фермента за счёт аллостерического эффекта, приводить к его инактивации (например, при связывании фермента с ингибитором) или к изменению специфичности фермента к своему субстрату[13].
Помимо этого, взаимодействие белков друг с другом может приводить к формированию нового центра связывания для субстрата на поверхности взаимодействия двух молекул. За счёт взаимодействия двух или более ферментов друг с другом становится возможным туннелирования субстрата[en], что увеличивает эффективность ферментативных реакций за счёт стабилизации интермедиатов и повышения их локальной концентрации[13].
Методы изучения белок-белковых взаимодействий[править | править код]
Существует множество методов изучения белок-белковых взаимодействий[13]. Некоторые из них позволяют экспериментально определять белки-партнёры для изучаемого белка, другие — лишь верифицировать возможное взаимодействие двух белков. Для подтверждения партнёрства двух белков используется бимолекулярная флуоресцентная комплементация (BiFC), FRET-методы, Far-Western, дрожжевая двугибридная система. Для решения задачи обнаружения белков-партнёров используется коиммунопреципитация с последующей аффинной хроматографией и масс-спектрометрией, система AviTag с промискуитетной BirA-лигазой. Основной проблемой в применении данных методов является возможная неспецифичность белка, который определился как входящий в состав белкового комплекса.
Дрожжевой двугибридный анализ[править | править код]
 Принципы в основе двугибридных систем для дрожжей и млекопитающих
Принципы в основе двугибридных систем для дрожжей и млекопитающихДвугибридные дрожжи позволяют in vivo выявлять парные ББВ (бинарный метод), а также неспецифичные липкие взаимодействия (sticky interactions)[14].
Клетки дрожжей трансфецируются двумя плазмидами: наживкой — интересующим нас белком с прилинкованным ДНК-связывающим доменом дрожжевого фактора транскрипции, например Gal4, и добычей — библиотекой кДНК (cDNA) фрагментов, прикреплённых к активирующему домену транскрипционного фактора. Если добыча и наживка взаимодействуют, два домена транскрипционного фактора соединяются и становятся функциональными. Таким образом, по присутствию результатов продукции репортерного гена можно судить о наличии взаимодействия между белками[6][15].
Несмотря на всю полезность, у дрожжевой двугибридной системы имеется ряд ограничений: относительно низкая специфичность; использование дрожжей в качестве основного хозяйского организма, что может приводить к проблемам при исследовании других биологических систем; относительно низкое количество обнаруживаемых ББВ, поскольку некоторые белки со слабыми связями теряются в процессе выделения[16] (к примеру, плохо обнаруживаются мембранные белки[17][18]). Ограничения преодолеваются использованием различных вариантов двугибридной системы, например мембранным дрожжевым двугибридом (membrane yeast two-hybrid)[18], сплит-убиквитиновыми системами[15], которые не ограничены взаимодействиями только внутри ядра; и бактериальными двугибридными системами (с использованием бактерий, соответственно)[19].
Афинная хроматография с последующей масс-спектрометрией[править | править код]
 Принцип тандемной аффиной хроматографии
Принцип тандемной аффиной хроматографииАффинная хроматография с последующей масс-спектрометрией позволяет обнаруживать, в основном, стабильные взаимодействия, тем самым лучше отражая функциональные ББВ, существующие в живой клетке (in vivo)[14][15]. При использовании этого метода сначала выделяют помеченный белок, экспрессируемый в клетке обычно в in vivo концентрациях, и взаимодействующие с ним белки (афинная хроматография). Один из наиболее выигрышных и широко используемых методов для выделения протеинов в случае сильного фонового загрязнения — это метод тандемной афинной хроматографии[en]. ББВ могут быть качественно и количественно проанализированы различными масс-спектрометрическими методами: химическим слиянием, биологическим или метаболическими слиянием (SILAC), или методами без использования меток[4].
Вычислительные способы предсказания ББВ[править | править код]
Так как до сих пор нет полных данных интерактома и не все ББВ обнаружены, при реконструкции сигнальных или метаболических карт взаимодействий используют различные вычислительные методы. Они позволяют устранить пробелы, предсказывая наличие тех или иных взаимодействий между узлами сети. С помощью вычислительных методов можно предсказать не только возможность ББВ, но также и их силу[2].
Ниже приведено несколько вычислительных подходов предсказания ББВ:
- Поиск событий слияния генов или доменов белков: слияния генов[en], что часто также означает слияние доменов, можно использовать для поиска функциональной связи между белками. При этом используется предположение, что слиянию этих генов в течение эволюции способствовал отбор[20].
- Методы сравнительной геномики и кластеризации генов: часто гены, которые кодируют белки со схожей функцией или взаимодействующие друг с другом белки, находятся в одном опероне (в случае бактерий) или совместно регулируются (корегуляция) (в случае эукариот). Такие гены обычно близко расположены в геноме. Методы кластеризации генов оценивают вероятность совместной встречаемости ортологов белков, которые кодируют гены из одного кластера. Такие подходы помогают выявлять скорее функциональное взаимодействие между белками, чем их физический контакт[2].
- Методы, основанные на филогенетических профилях: в таких методах предполагают, что если негомологичные белки функционально связаны, то существует вероятность того, что они могут вступать в ББВ и коэволюционировать. Для того чтобы найти функциональную связь между белками, используют кластеризацию по филогенетическим профилям[en] этих белков или же оценивают вероятность совместной встречаемости белков в различных протеомах[2]. Идея того, что у взаимодействующих друг с другом белков часто схожие по топологии филогенетические деревья, используется в методе «mirror tree»[21].
- Способы предсказания на основе гомологии: данный подход предполагает, что исследуемые белки будут взаимодействовать друг с другом, если известно, что их гомологи вступают во взаимодействие. Такие пары белков из разных организмов, которые сохранили в течение эволюции способность взаимодействовать друг с другом, называются интерологами[en]. Примерами сервисов, использующих данный метод, являются PPISearch и BIPS[2].
- Предсказание, основанное на данных коэкспрессии генов: если исследуемые белки кодируют гены с похожими паттернами экспрессии (схожий профиль и уровень экспрессии) в разные временные промежутки, то можно предположить, что эти белки функционально связаны и, возможно, как-то взаимодействуют друг с другом[22].
- Методы на основе сетевой топологии: сети ББВ можно представить в виде графа, где узлами являются белки, а каждое ребро обозначает взаимодействие между белками. С помощью математической интерпретации сети ББВ (например, в виде матрицы смежности) можно определить, как белки функционально связаны между собой, а также предсказать новые ББВ. Если у двух белков очень много общих партнёров в сети, то скорее всего они принимают участие в одном биологическом процессе и потенциально могут взаимодействовать друг с другом[2].
- In-Silico Two-Hybrid подход: главное предположение данного метода — взаимодействующие друг с другом белки коэволюционируют, чтобы сохранить функциональность. Данный метод анализирует множественные выравнивания белкового семейства и ищет скоррелированные мутации для предсказания ББВ и поиска оснований, входящих в участок связывания[23].
- Предсказание ББВ, основанное на структуре белков: такой подход позволяет не только выяснить, могут ли белки взаимодействовать, но и охарактеризовать это взаимодействие (например, его физические характеристики или аминокислоты, входящие в состав поверхности взаимодействия двух белков). Одним из методов, использующих трёхмерную структуру белков, является докинг. Сюда же относят методы, которые предполагают эволюционную консервативность оснований, входящих в состав поверхности взаимодействия. Таким образом, на основе уже известных структур можно предсказать, как будет выглядеть мультимолекулярный комплекс исследуемых белков[2].
- Методы, основанные на машинном обучении или интеллектуальном анализе текста: на основе машинного обучения был разработан метод предсказания ББВ, который использует только последовательности исследуемых белков[24]. Это позволяет проанализировать, хотя и менее точно, бóльшее число возможных взаимодействий, так как для работы используются только аминокислотные последовательности. Интеллектуальный анализ текста ищет связь между белками, рассматривая их взаимное упоминание в предложениях или параграфах различных текстовых блоков[25].
Крупномасштабные поиски ББВ позволили выявить сотни тысяч взаимодействий, информация о которых была собрана в специализированных биологических базах данных (БД). Эти базы постоянно обновляются с целью предоставить полный интерактом. Первой такой базой стала База Данных Взаимодействующих Белков(DIP)[en][26]. С момента её появления число публичных баз данных продолжает расти. Эти БД можно разделить на три класса: первичные, мета-БД и БД предсказаний[1].
- Первичные БД собирают информацию об опубликованных ББВ, чье существование доказано в мелко- или крупномасштабных экспериментах. Например, к ним можно отнести DIP, Biomolecular Interaction Network Database (BIND), Biological General Repository for Interaction Datasets (BioGRID), Human Protein Reference Database (HPRD), IntAct Molecular Interaction Database, Molecular Interactions Database (MINT), MIPS Protein Interaction Resource on Yeast (MIPS-MPact) и MIPS Mammalian Protein-Protein Interaction Database (MIPS-MPPI)[1].
- Мета-БД обычно являются результатом объединения данных из первичных баз, но могут и впоследствии пополняться оригинальной информацией. Примеры: Agile Protein Interaction DataAnalyzer (APID), The Microbial Protein Interaction Database (MPID8) и Protein Interaction Network Analysis (PINA) platform[1].
- БД предсказанных ББВ заполняются результатами, полученными с использованием различных техник. Примеры: Michigan Molecular Interactions (MiMI), Human Protein-Protein Interaction Prediction Database (PIPs), Online Predicted Human Interaction Database (OPHID), Known and Predicted Protein-Protein Interactions (STRING), а также Unified Human Interactome (UniHI)[1].
 Визуализация интерактома человека, где точки обозначают белки, а соединяющие их синие линии — взаимодействия между белками
Визуализация интерактома человека, где точки обозначают белки, а соединяющие их синие линии — взаимодействия между белкамиИнформация, содержащаяся в базах ББВ, позволяет строить сети белковых взаимодействий. Сеть ББВ для одного конкретного белка вполне возможно описать, например, с помощью текста. Но задача создания диаграммы всевозможных внутриклеточных ББВ поистине сложна и трудноизобразима. Одним из примеров вручную созданной молекулярной карты взаимодействий является карта контроля клеточного цикла, созданная Куртом Коном (Kurt Kohn) в 1999 году[27]. Базируясь на карте Кона, Швиковски (Schwikowski) и др. в 2000 году опубликовали карту ББВ в дрожжах, объединившую 1548 взаимодействующих протеина, информация о которых была получена методом двугибридного анализа. При визуализации для первоначального расположения вершин использовался метод послойного изображения графа, а затем полученное изображение было улучшено за счет применения силового (force based) алгоритма[28][29].
Чтобы упростить сложную задачу визуализации, были разработаны различные биоинформатические инструменты, которые также позволяют сочетать информацию о ББВ с другими типами данных. К примеру, широко используется пакет с открытым исходным кодом Cytoscape, к которому доступна масса плагинов[1][30]. Для визуализации и анализа очень больших сетей подходит пакет Pajek[31].
Важная роль ББВ в физиологических и патологических процессах является хорошей мотивацией для расширения интерактома. В качестве примеров уже опубликованных интерактомов можно привести thyroid-специфичный интерактом DREAM[32] и PP1α-интеракто в человеческом мозге[33].
- ↑ 1 2 3 4 5 6 7 8 9 De Las Rivas, J.; Fontanillo, C. Protein-protein interactions essentials: key concepts to building and analyzing interactome networks (англ.) // PLoS computational biology : journal. — 2010. — Vol. 6, no. 6. — P. e1000807. — PMID 20589078.
- ↑ 1 2 3 4 5 6 7 8 9 10 Keskin, O.; Tuncbag, N; Gursoy, A. Predicting Protein–Protein Interactions from the Molecular to the Proteome Level (англ.) // Chemical Reviews (англ.)русск. : journal. — 2016. — Vol. 116, no. 8. — P. 4884—4909. — PMID 27074302.
- ↑ Herce, H.D.; Deng, W.; Helma, J.; Leonhardt, H.; Cardoso, M.C. Visualization and targeted disruption of protein interactions in living cells (англ.) // Nature Communications (англ.)русск. : journal. — Nature Publishing Group, 2013. — Vol. 4. — P. 2660. — PMID 24154492.
- ↑ 1 2 Jones, S.; Thornton, J.M. Principles of protein-protein interactions (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 1996. — Vol. 93, no. 1. — P. 13—20. — PMID 8552589.
- ↑ Nooren, I.M.; Thornton, J.M. Diversity of protein-protein interactions (англ.) // EMBO J. (англ.)русск. : journal. — 2003. — Vol. 22, no. 14. — P. 3486—3492. — PMID 12853464.
- ↑ 1 2 Westermarck, J.; Ivaska, J.; Corthals, G.L. Identification of protein interactions involved in cellular signaling (англ.) // Molecular & cellular proteomics : MCP : journal. — 2013. — Vol. 12, no. 7. — P. 1752—1763. — PMID 23481661.
- ↑ Janin J., Chothia C. The structure of protein-protein recognition sites. (англ.) // The Journal of biological chemistry. — 1990. — Vol. 265, no. 27. — P. 16027—16030. — PMID 2204619.
- ↑ 1 2 Bruce, A.; Johnson, A.; Lewis, J.; Raff, M.; Roberts, K.; Walter, P. Molecular biology of the cell (неопр.). — 4th. — New York: Garland Science (англ.)русск., 2002. — ISBN 0-8153-3218-1.
- ↑ Kendrew, J.C.; Bodo, G.; Dintzis, H.M.; Parrish, R.G.; Wyckoff, H.; Phillips, D.C. A three-dimensional model of the myoglobin molecule obtained by x-ray analysis (англ.) // Nature : journal. — 1958. — Vol. 181, no. 4610. — P. 662—666. — PMID 13517261.
- ↑ Wand, A.J.; Englander, S. W. Protein complexes studied by NMR spectroscopy (неопр.) // Current opinion in biotechnology. — 1996. — Т. 7, № 4. — С. 403—408. — PMID 8768898.
- ↑ Vinogradova, O.; Qin, J. NMR as a unique tool in assessment and complex determination of weak protein-protein interactions (англ.) // Topics in current chemistry : journal. — 2012. — Vol. 326. — P. 35—45. — PMID 21809187.
- ↑ Berridge, M.J. Cell Signalling Biology: Module 6 – Spatial and Temporal Aspects of Signalling (англ.) // Biochemical Journal (англ.)русск. : journal. — 2012. — DOI:10.1042/csb0001006.
- ↑ 1 2 3 Phizicky E. M., Fields S. Protein-protein interactions: methods for detection and analysis. (англ.) // Microbiological reviews. — 1995. — Vol. 59, no. 1. — P. 94—123. — PMID 7708014.
- ↑ 1 2 Brettner L. M., Masel J. Protein stickiness, rather than number of functional protein-protein interactions, predicts expression noise and plasticity in yeast. (англ.) // BMC systems biology. — 2012. — Vol. 6. — P. 128. — DOI:10.1186/1752-0509-6-128. — PMID 23017156.
- ↑ 1 2 3 Wodak, S.J.; Vlasblom, J.; Turinsky, A.L.; Pu, S. Protein-protein interaction networks: the puzzling riches (англ.) // Current opinion in structural biology : journal. — 2013. — Vol. 23, no. 6. — P. 941—953. — PMID 24007795.
- ↑ Rajagopala, S.V.; Sikorski, P.; Caufield, J.H.; Tovchigrechko, A.; Uetz, P. Studying protein complexes by the yeast two-hybrid system (англ.) // Methods : journal. — 2012. — Vol. 58, no. 4. — P. 392—399. — PMID 22841565.
- ↑ Stelzl, U.; Wanker, E.E. The value of high quality protein-protein interaction networks for systems biology (англ.) // Current opinion in chemical biology : journal. — 2006. — Vol. 10, no. 6. — P. 551—558. — PMID 17055769.
- ↑ 1 2 Petschnigg, J.; Snider, J.; Stagljar, I. Interactive proteomics research technologies: recent applications and advances (англ.) // Current opinion in biotechnology : journal. — 2011. — Vol. 22, no. 1. — P. 50—8. — PMID 20884196.
- ↑ Battesti, A; Bouveret, E. The bacterial two-hybrid system based on adenylate cyclase reconstitution in Escherichia coli (англ.) // Methods : journal. — 2012. — Vol. 58, no. 4. — P. 325—334. — PMID 22841567.
- ↑ Enright, A. J.; Iliopoulos, I.; Kyrpides, N.C.; Ouzounis, C.A. Protein Interaction Maps for Complete Genomes Based on Gene Fusion Events (англ.) // Nature : journal. — 1999. — Vol. 402, no. 6757. — P. 86—90. — PMID 10573422.
- ↑ Pazos, F.; Valencia, A. Similarity of Phylogenetic Trees as Indicator of Protein-Protein Interaction (англ.) // Protein Eng., Des. Sel. : journal. — 2001. — Vol. 14, no. 9. — P. 609—614. — PMID 11707606.
- ↑ Jansen, R.; IGreenbaum, D.; Gerstein, M. Relating Whole- Genome Expression Data with Protein-Protein Interactions (англ.) // Genome Res. (англ.)русск. : journal. — 2002. — Vol. 12, no. 1. — P. 37—46. — PMID 11779829.
- ↑ Pazos, F.; Valencia, A. In Silico Two-Hybrid System for the Selection of Physically Interacting Protein Pairs (англ.) // Proteins: Struct., Funct., Genet. : journal. — 2002. — Vol. 47, no. 2. — P. 219—227. — PMID 11933068.
- ↑ Shen, J.; IZhang, J.; Luo, X.; Zhu, W.; Yu, K.; Chen, K.; Li, Y.; Jiang, H. Predicting protein-protein interactions based only on sequences information (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2007. — Vol. 104, no. 11. — P. 4337—4341. — PMID 17360525.
- ↑ Papanikolaou, N.; Pavlopoulos, G.A.; Theodosiou, T.; Iliopoulos, I. Protein-protein interaction predictions using text mining methods (англ.) // Methods : journal. — 2015. — Vol. 74. — P. 47—53. — PMID 25448298.
- ↑ Xenarios I., Rice D. W., Salwinski L., Baron M. K., Marcotte E. M., Eisenberg D. DIP: the database of interacting proteins. (англ.) // Nucleic acids research. — 2000. — Vol. 28, no. 1. — P. 289—291. — PMID 10592249.
- ↑ Schwikowski B., Uetz P., Fields S. A network of protein-protein interactions in yeast. (англ.) // Nature biotechnology. — 2000. — Vol. 18, no. 12. — P. 1257—1261. — DOI:10.1038/82360. — PMID 11101803.
- ↑ Rigaut G., Shevchenko A., Rutz B., Wilm M., Mann M., Séraphin B. A generic protein purification method for protein complex characterization and proteome exploration. (англ.) // Nature biotechnology. — 1999. — Vol. 17, no. 10. — P. 1030—1032. — DOI:10.1038/13732. — PMID 10504710.
- ↑ Prieto C., De Las Rivas J. APID: Agile Protein Interaction DataAnalyzer. (англ.) // Nucleic acids research. — 2006. — Vol. 34. — P. 298—302. — DOI:10.1093/nar/gkl128. — PMID 16845013.
- ↑ Michael Kohl, Sebastian Wiese, and Bettina Warscheid (2011) Cytoscape: Software for Visualization and Analysis of Biological Networks. In: Michael Hamacher et al. (eds.), Data Mining in Proteomics: From Standards to Applications, Methods in Molecular Biology, vol. 696, DOI 10.1007/978-1-60761-987-1_18
- ↑ Raman, K. Construction and analysis of protein-protein interaction networks (англ.) // Automated experimentation : journal. — 2010. — Vol. 2, no. 1. — P. 2. — PMID 20334628.
- ↑ Rivas, M.; Villar, D.; González, P.; Dopazo, X.M.; Mellstrom, B.; Naranjo, J.R. Building the DREAM interactome (неопр.) // Science China. Life sciences. — 2011. — Т. 54, № 8. — С. 786—792. — PMID 21786202.
- ↑ Esteves, S.L.; Domingues, S.C.; da Cruz e Silva, O.A.; Fardilha, M.; da Cruz e Silva, E.F. Protein phosphatase 1α interacting proteins in the human brain (англ.) // Omics : a journal of integrative biology : journal. — 2012. — Vol. 16, no. 1—2. — P. 3—17. — PMID 22321011.
