– свойства белков – Биохимия
К физико-химическим свойствам белков относят амфотерность, растворимость, способность к денатурации, коллоидные свойства.
Амфотерность
Так как белки содержат кислые и основные аминокислоты, то в их составе всегда имеются свободные кислые (СОО–) и основные (NH3+) группы.
Заряд белка зависит от соотношения количества кислых и основных аминокислот. Поэтому, аналогично аминокислотам, белки заряжаются положительно при уменьшении рН, и отрицательно при его увеличении. Если рН раствора соответствует изоэлектрической точке белка, то заряд белка равен 0.
Если в пептиде или белке преобладают основные аминокислоты (лизин и аргинин), то при нейтральных рН заряд белка положительный, т.к. обусловлен положительным зарядом радикала этих аминокислот.
Если в белке преобладают кислые аминокислоты (глутамат и аспартат), то белок кислый, при нейтральных рН заряд белка отрицательный и изоэлектрическая точка находится в кислой среде. Для большинства природных белков изоэлектрическая точка находится в диапазоне рН 4,8-5,4, что свидетельствует о преобладании в их составе глутаминовой и аспарагиновой аминокислот.
Для большинства природных белков изоэлектрическая точка находится в диапазоне рН 4,8-5,4, что свидетельствует о преобладании в их составе глутаминовой и аспарагиновой аминокислот.
Амфотерность имеет значение для выполнения белками некоторых функций. Например, буферные свойства белков, т.е. способность поддерживать стабильность рН крови, основаны на способности присоединять ионы Н+ при закислении среды или отдавать их при защелачивании.
С практической стороны наличие амфотерности позволяет разделять белки по заряду (электрофорез) или использовать изменение величины рН раствора для осаждения какого-либо известного белка. Наличие как положительных, так и отрицательных зарядов в белке обусловливает их способность к высаливанию, что удобно для выделения белков в нативной (живой) конформации.
Влияние рН на заряд белка
При смещении рН в растворе изменяется концентрация ионов Н+. При закислении среды (при снижении рН) ниже изоэлектрической точки ионы Н+ присоединяются к отрицательно заряженным группам глутаминовой и аспарагиновой кислот и нейтрализуют их. Заряд белка при этом становится положительным.
При закислении среды (при снижении рН) ниже изоэлектрической точки ионы Н+ присоединяются к отрицательно заряженным группам глутаминовой и аспарагиновой кислот и нейтрализуют их. Заряд белка при этом становится положительным.
При увеличении рН в растворе выше изоэлектрической точки концентрация ионов Н+ снижается и положительно заряженные группы белка (NH3+-группы лизина и аргинина) теряют протоны, их заряд исчезает. Суммарный заряд белка становится отрицательным.
Изменение заряда белковой цепи при изменении pH
Растворимость
Так как большинство белков несет много заряженных групп, то в целом они водорастворимы. Растворимость объясняется:
- наличием заряда и взаимоотталкиванием заряженных молекул белка,
- наличием гидратной оболочки – окружение молекулы диполями воды и взаимодействие их с полярными и заряженными группами на поверхности глобулы белка. Чем больше полярных и/или заряженных аминокислот в белке, тем больше гидратная оболочка.

Например, 100 г белка альбумина связывает 30-50 г воды.
Белки. Строение, свойства, качественные реакции – методическая разработка для учителей, Бейсенбекова Гульзия Сапарбековна
|
Цели обучения, которые достигаются на данном уроке (ссылка на учебную программу): |
10.5.1.3 знать значение аминокислот; 10.5.1.4 исследовать процесс гидролиза белков и доказывать наличие аминокислот в их составе. |
|
|
Цели урока: |
Учащиеся будут: – объяснять схему пищевой пирамиды; – знать, что 20 аминокислот существенные для жизни человека; – записывать структуру нескольких аминокислот и указывать на их связь с органическими кислотами; – проводить анализ реакции поликонденсации между аминокислотами с образованием белка; – используют бумажную хроматографию для разделения аминокислот и строят хроматограмму с помощью нингидрина. |
|
|
|
Навыки |
Критерии успеха |
|
10.5.1.3 знать значение аминокислот; |
Знание и понимание: |
– дает верное определение аминокислот; – правильно распределяет 8-10 аминокислот на заменимые и незаменимые. |
|
10.5.1.4 исследовать процесс гидролиза белков и доказывать наличие аминокислот в их составе. |
Критическое мышление и исследование: |
Учащийся достиг цели обучения, если: |
|
|
|
– разделяет аминокислоты с помощью бумажной хроматографии с использованием Нингидрина; – проводит расчёт значений Rf; – определяет аминокислотный состав раствора гидролизованного белка, сравнив полученные значения с опорными значениями Rf. |
|
Языковые цели: |
Учащиеся могут: знать о составе белков, о названиях некоторых аминокислот, объяснять амидную связь. Предметная лексика и терминология: заменимые и незаменимые аминокислоты, функциональные группы, карбоксильная и аминогруппы, бифункциональное соединение. Серия полезных фраз для диалога/письма: Пептидная или амидная группа образуется между…………………………………группами при реакции поликонденсации. Белки состоят из остатков…………. аминокислот; Пептиды, содержащие …….. …….. ……….. …………………., соединенных пептидными связями. Белки……………….. важная органическая молекула, ……………. … ……. ……аминокислотных остатков, соединенных пептидной связью. |
|
|
Привитие ценностей: |
– уважение друг другу при выполнении парной работы; – сотрудничество при групповой работе; – открытость выражения мыслей, идей при обсуждении вопросов; – труд и творчество при выполнении практической работы; – обучение на протяжении всей жизни. |
|
|
Межпредметные связи: |
межпредметная интеграция на уроке с предметом биология осуществляется через самообучение учащихся при выполнении домашнего задания: «Содержание белков, жиров, углеводов в продуктах питания». |
|
|
Предварительные знания: |
Соединения углерода 1 (6.3С) Поведение электронов в атомах (8.2A) Углерод и его соединения (8.4В) Структура элементов и соединений (9.1В) Введение в органическую химию (10.3А) Углеводороды (10.3B) |
|
Ход урока
|
Запланированные этапы урока |
Запланированная деятельность на уроке |
Ресурсы |
||||||||||||||||
|
Начало урока 7 минут |
Приветствие. Индивидуальная работа. Учащимся раздать рабочие листы с тестовыми заданиями «RUTwig_Основы питания_Тест», на которые ответят во время просмотра видеоматериала «Основы питания: Белки». Вопросы: A – 10-15% B – 30-35% C – 50-55% D – 70-75% 2.Что из этих пищевых продуктов НЕ является источником белка? A – мясо B – рыба C – яйца D – сахар 3.В состав всех белков входят: A – углерод, азот и кислород B – углерод, азот и водород C – углерод, водород, фосфор и кислород D – углерод, водород, кислород и азот 4. A – аминокислоты B – сахара C – жиры D – углеводы 5.Что из перечисленного НЕ является функцией белков? A – рост и восстановление клеток B – гормоны C – ферменты D – термоизоляция 6. Во время пищеварения белки распадаются на: A – жирные кислоты B – глюкозу C – крахмал D – аминокислоты 7.Какое из этих утверждений НЕВЕРНОЕ? A – ферменты – это белки B – волосы состоят из белков C – белки могут быть источником энергии D – наш организм может синтезировать важные аминокислоты 8. A – переваривание белка начинается во рту B – соляная кислота в желудке расщепляет белки C – ферменты, называемые протеазами, расщепляют белки в желудке и кишечнике D – аминокислоты всасываются в кровь Обсуждение видеоматериала и дополнение ответов. Устное оценивание ответов учащихся. Поощрение учащегося, ответившего на все вопросы правильно. Подвести учащихся к теме урока: |
Интерактивная доска https://twig-bilim.kz/film/food-basics-proteins-6552/ «Основы питания: Белки» Рабочие листы
|
||||||||||||||||
|
Середина урока 8 мин |
Тема урока: Белки, строение, свойства, качественные реакции. Вопросы учащимся:
Обсуждая, направить учащихся на выведение цели обучения и критерии успеха. Учащиеся формулируют цели обучения, которую достигнут в течении урока и составляют словесный план достижения ЦО. Просмотр видеоматериала с образовательного ресурса twig-bilim.kz. «Аминокислоты». Обсуждение с классом основных понятий, запись в тетради. Ключевые слова:
Парная работа Предоставить учащимся ноутбуки. Задание:
Использование информации с образовательного ресурса bilimland.kz «Раздел Белки. Белки в нашем рационе питания» Главную роль при составлении карты играют два момента: 1.ЦветИспользование цвета в процессе обучения значительно облегчает усвоение информации. Яркий цвет позволяет выделить нужные моменты, привлекая к ним внимание, включает творческое мышление и найти самую актуальную информацию. Например, выделение цветом важных моментов увеличивает внимание на 80%, а желтый цвет стимулирует мозговую деятельность. 2. ОбразыСвязывание содержания текста с возникающими образами помогает лучше понять сам текст. По окончании выполнения ментальной карты, выслушать на выбор две пары. Первая пара презентует заменимые аминокислоты, вторая пара – незаменимые аминокислоты. Обсуждение и дополнение ответов учащихся. |
Интерактивная доска https://twig-bilim.kz/film/glossary/amino-acid-5592/
https://bilimland.
Рабочий лист
Ментальная карта — примеры составления «Ментальная карта – примеры составления»
|
||||||||||||||||
|
8 мин |
Групповая работа. Учащиеся получают информационные карточки. Обсуждая полученную информацию, делятся на три группы: «Аминокислота», «Белок», «Пептиды». Каждая группа, обсудив, отвечает на вопрос по названию группы:
Задание. Записать образования белка из аминокислот реакцией поликонденсации. 1-группа: образование дипепетида из глицина и аспарагиновой кислоты; 2-группа: образование дипепетида из цистеина и глутаминовой кислоты; 3-группа: образование дипепетида из аланина и лизина; Для выполнения задания учащиеся используют информационный материал с образовательного ресурса bilimland.kz, «Раздел Аминокислоты. Аминокислоты, содержащие в белках» После выполнения задания, группы объединяются в две команды и получают трипептид из данных аминокислот. Процесс взаимооценивания. Обзор учащимися ответов одноклассников. Обсуждение и дополнение ответов. |
https://bilimland.kz/ru/courses/chemistry-ru/organicheskaya-ximiya/azotsoderzhashie-organicheskie-soedineniya/lesson/aminokisloty «Раздел Аминокислоты. Аминокислоты, содержащие в белках» |
||||||||||||||||
|
13 мин |
Парная работа. Лабораторная работа «Определение наличия аминокислот в белке». Цель:………………………………………………….. Введение:………………………………………………………. Гипотеза:……………………………………………………….. Методы:………………………………………………………….Реактивы:……………………………………………………….Оборудование:………………………………………………..Ход работы: Просмотр видеоматериала с образовательного ресурса Bilimland.kz. Записывают наблюдения в тетради. – Даны растворы аминокислот: глицина, изолейцина, серина, фениаланина. Запишите наблюдения. – Капля раствора наносится в нижнюю часть алюминиевого листа покрытого тонким слоем силикогеля. – На одинаковом расстоянии у основания листа одновременно нанесите каплю известных аминокислот. Дайте высохнуть листу. Запишите наблюдения. – Лист опустить в раствор, в составе которого содержится: 40% трихлорметана; 40% метанола,20% водного раствора аммиака. Запишите наблюдения. – Нанесенные точки аминокислот перемещаются с раствором с различной скоростью. Пятна достигают разной высоты. Запишите наблюдения. – Когда хроматограмма готова, опрыскивают ее раствором Нингидрина. Это соединение при высокой температуре дает окрашенные продукты. Запишите наблюдения.
Для определения применяют справо чную даннуюзначения Rf Вывод: аминокислоты можно различить и идентифицировать с помощью аналитического метода, называемого тонкослойной хроматографией. Теоретический материал.
Rf = Расстояние, пройденное чернилой / Расстояние, пройденное растворителем. Это называется Rf значением для конкретной чернилы, и различные чернила будут иметь разные значения Rf и, таким образом, их можно различать друг от друга. Все типы хроматографии зависят от перемещения (типа) растворителя, известной в качестве подвижной фазы, и от того, что удерживает компоненты смеси, известной в качестве стационарной фазы. В бумажной хроматографии подвижной фазой является вода, а стационарной фазой – бумага. |
Рабочая тетрадь Рабочий лист https://bilimland. |
||||||||||||||||
|
Конец урока 37-39 мин |
В конце урока учащиеся проводят рефлексию по целям обучения, критериям успеха. – Я научился(лась) выполнять расчеты …………………………………………………………………… – Я узнал(а) о строении белка ………………………………………………………….. – Мне остался непонятным процесс исследования строения………………………………………………. – Мне необходимо поработать с учебным материалом………………………………………….. |
Рабочая тетрадь |
||||||||||||||||
|
Домашнее задание 40 мин |
Для закрепления материала, решить задачи №1, 4, 5 с образовательного ресурса itest.
|
https://itest.kz/ru/himia-ru Рабочая тетрадь |
Белки — физические и химические свойства
Присоединяйся сейчас
Если вы готовы сдать экзамены по биологии уровня A, станьте участником прямо сейчас, чтобы получить полный доступ ко всей нашей библиотеке материалов для повторения.
Присоединяйтесь к более чем 22 000 учащихся, сдавших экзамены благодаря нам!
Зарегистрируйтесь ниже, чтобы получить мгновенный доступ!
Присоединиться →
Или попробуйте пример…
Еще не готовы приобрести комплект для доработки? Без проблем. Если вы хотите ознакомиться с тем, что мы предлагаем, перед покупкой, у нас есть бесплатная подписка с образцами материалов для пересмотра.
Зарегистрируйтесь в качестве бесплатного члена ниже, и вы вернетесь на эту страницу, чтобы попробовать образцы материалов перед покупкой.
Скачать образцы →
Физические свойства белков- Цвет и вкус
Белки бесцветны и обычно не имеют вкуса. Они однородные и кристаллические. - Форма и размер
Форма белков варьируется от простых кристаллоидных сферических структур до длинных фибриллярных структур. Были распознаны два различных образца формы
:
A. Глобулярные белки- Они имеют сферическую форму и встречаются в основном в растениях, особенно в семенах и клетках листьев. Это пучки, образованные складыванием и смятием белковых цепей. например, пепсин, эдестин, инсулин, рибонуклеаза и т. д.
B. Фибриллярные белки — Они имеют нитевидную или эллипсоидальную форму и обычно встречаются в мышцах животных. Большинство исследований структуры белка было проведено с использованием этих белков. например, фибриноген, миозин и т. д.
Большинство исследований структуры белка было проведено с использованием этих белков. например, фибриноген, миозин и т. д. - Молекулярная масса
Белки обычно имеют большую молекулярную массу в диапазоне от 5 × 103 до 1 × 106. Следует отметить, что значения молекулярной массы многих белков близки или кратны 35 000 и 70 000. - Коллоидная природа
Из-за своего гигантского размера белки обладают многими коллоидными свойствами, такими как; Скорость их диффузии чрезвычайно мала, и они могут вызывать значительное светорассеяние в растворе, что приводит к видимой мутности (эффект Тиндаля). - Денатурация
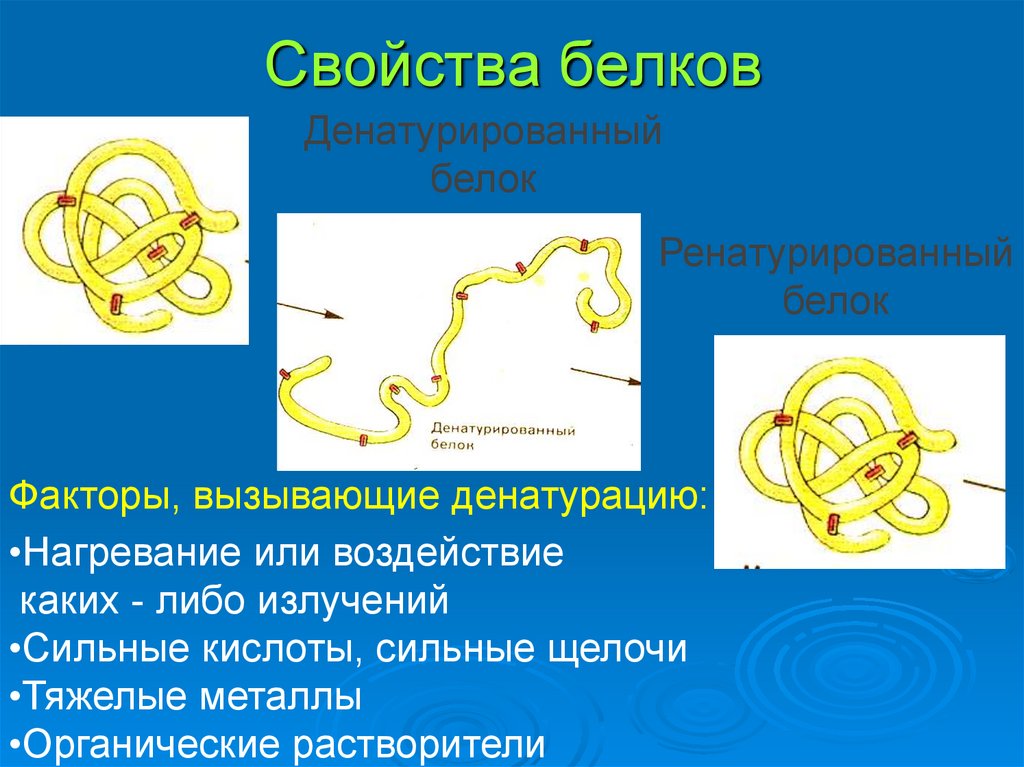
Денатурация относится к изменениям свойств белка. Другими словами, это потеря биологической активности. Во многих случаях за процессом денатурации следует коагуляция — процесс, при котором денатурированные белковые молекулы имеют тенденцию образовывать большие агрегаты и осаждаться из раствора. - Амфотерная природа
Как и аминокислоты, белки амфотерны, т. е. действуют как кислоты и щелочи. Они мигрируют в электрическом поле, и направление миграции зависит от суммарного заряда, которым обладает молекула. На чистый заряд влияет значение pH. Каждый белок имеет фиксированное значение изоэлектрической точки (pl), при которой он будет двигаться в электрическом поле.
е. действуют как кислоты и щелочи. Они мигрируют в электрическом поле, и направление миграции зависит от суммарного заряда, которым обладает молекула. На чистый заряд влияет значение pH. Каждый белок имеет фиксированное значение изоэлектрической точки (pl), при которой он будет двигаться в электрическом поле. - Способность связывать ионы
Белки могут образовывать соли как с катионами, так и с анионами в зависимости от их суммарного заряда. - Растворимость
На растворимость белков влияет рН. Растворимость самая низкая в изоэлектрической точке и увеличивается с увеличением кислотности или щелочности. Это связано с тем, что когда белковые молекулы существуют в виде катионов или анионов, силы отталкивания между ионами велики, поскольку все молекулы обладают избыточными зарядами одного знака. Таким образом, они будут более растворимы, чем в изоэлектрическом состоянии. - Оптическая активность
Все белковые растворы поворачивают плоскость поляризованного света влево, т. е. являются левораторными.
е. являются левораторными.
- Гидролиз
Белки гидролизуются различными гидролитическими агентами.
A. Кислотными агентами: Белки при гидролизе с конц. HCl (6–12 н.) при 100–110°С в течение 6–20 ч дают аминокислоты в виде их гидрохлоридов.
B. С помощью щелочных агентов: белки также можно гидролизовать с помощью 2 н. NaOH. - Реакции с участием СООН группы
A. Реакции со щелочами (Солеобразование)
B. Реакции со спиртами (Этерификация)
C. Реакции с аминами - Реакции с участием Nh3 группы
A. Реакции с минеральными кислотами образование): когда свободные аминокислоты или белки обрабатывают минеральными кислотами, такими как HCl, образуются кислые соли.
B. Реакция с формальдегидом: С формальдегидом образуются гидроксиметилпроизводные.
C. Реакция с бензальдегидом: образуются основания Шиффа
D. Реакция с азотистой кислотой (реакция Ван Слайка): Аминокислоты реагируют с HNO2 с выделением газообразного N2 и образованием соответствующих α-гидроксикислот.
Реакция с азотистой кислотой (реакция Ван Слайка): Аминокислоты реагируют с HNO2 с выделением газообразного N2 и образованием соответствующих α-гидроксикислот.
E. Реакция с ацилирующими агентами (ацилирование)
F. Реакция с FDNB или реагентом Сенгера
G. Реакция с дансилхлоридом - Реакции с участием группы COOH И Nh3
A. Реакция с трикетогидринденгидратом (9-нингидриновая реакция)0030 B. Реакция с фенилизоцианатом: С фенилизоцианатом образуется гидантоиновая кислота, которая, в свою очередь, может быть преобразована в гидантоин.
C. Реакция с фенилизотиоцианатом или реактивом Эдмана
D. Реакция с фосгеном: С фосгеном образуется N-карбоксиангидрид
E. Реакция с сероуглеродом: С сероуглеродом образуется 2-тио-5-тиозолидон - Реакции с участием группы R или боковой цепи
A. Биуретовый тест
B. Ксантопротеидный тест
C. Тест Миллона
D. Реакция Фолина
E. Реакция Сакагути
F. Реакция Паули
Реакция Паули
G. Реакция Эрлиха - Реакции с участием группы SH
A. Реакция на нитропруссид: Нитропруссид натрия в разбавленном растворе Nh5.OH окрашивается в красный цвет. Тест специфичен для цистеина.
B. Тест Салливана: цистеин окрашивается в красный цвет в присутствии 1,2-нафтохинон-4-сульфоната натрия и гидросульфита натрия.
Функции, структура, свойства и классификация
РЕКЛАМА:
Проведем углубленное изучение белков. Прочитав эту статью, вы узнаете: 1. Функции белков 2. Структуры белков 3. Свойства белков и 4. Классификация белков.
Белки представляют собой азотсодержащие органические соединения с высокой молекулярной массой, которые играют жизненно важную или первостепенную роль в живых организмах. Они состоят из 20 стандартных а-аминокислот.
Функции белков:Основные функции белков в организме человека:
РЕКЛАМА:
1. Они служат единицами бодибилдинга, например, мышечными белками.
Они служат единицами бодибилдинга, например, мышечными белками.
2. Обеспечивают поддержку и защиту различных тканей, например, коллагена и кератина.
3. Все химические реакции в организме катализируются белковыми ферментами, например трипсином.
4. Переносят различные молекулы и ионы из одного органа в другой, например, гемоглобин, сывороточный альбумин.
РЕКЛАМА:
5. Они хранят и обеспечивают питательные вещества, например молочный казеин, яичный альбумин.
6. Защищают организм от вредных инородных организмов, например, иммуноглобулины, фибриноген.
7. Они помогают регулировать клеточную или физиологическую активность, например, гормонов, а именно инсулина, ГР.
Структуры белков: Первичная структура белков :Первичная структура белков относится к общему количеству аминокислот и их последовательности в данном конкретном белке.
Определенное количество аминокислот расположены в определенной последовательности. Последовательность аминокислот в белке определяет его биологическую роль. Различные белки имеют разные последовательности. Поэтому изучение общего числа и последовательности аминокислот в белке есть изучение его первичной структуры.
Последовательность аминокислот в белке определяет его биологическую роль. Различные белки имеют разные последовательности. Поэтому изучение общего числа и последовательности аминокислот в белке есть изучение его первичной структуры.
Первичная структура отличает нормальный белок от аномального. Нормальный взрослый гемоглобин (HbA) состоит из 2 α-цепей и 2 β-цепей. Каждая α-цепь состоит из 141 аминокислоты, а каждая β-цепь состоит из 146 аминокислот, расположенных в определенной последовательности. Любое изменение в последовательности приводит к аномальному гемоглобину. Как и в серповидноклеточном гемоглобине (HbS), аминокислота валин присутствует в 6-м положении Р-цепи вместо глутаминовой кислоты в нормальном гемоглобине.
Вторичная структура белков :Это относится к скручиванию полипептидной цепи в спиральную форму.
Встречаются три типа спиральных структур:
РЕКЛАМА:
(а) Альфа-спираль
(b) Бета со складками и
(c) Обратный поворот.
1. Альфа-спираль:
РЕКЛАМА:
α означает первую, и структура, описанная ниже, была первой среди обнаруженных спиральных структур, поэтому она известна как альфа (α) спираль.
Отличительные особенности этой структуры:
я. Здесь полипептид закручивается или скручивается, образуя правостороннюю спиральную структуру.
ii. Расстояние между каждым витком катушки равно 5,4 Å.
РЕКЛАМА:
III. На виток приходится 3,6 аминокислоты.
ив. Группы «R» видны выступающими из спирали.
v. Имеются внутрицепочечные водородные связи, при которых водород группы -NH соединяется с кислородом группы -СО 4-й аминокислоты позади нее. Таким образом, каждая пептидная группа участвует в водородных связях.
в.и. Этот тип структуры встречается во многих белках в сочетании с другими структурами. Чистая а-спиральная структура наблюдается в белке волос, то есть в кератине.
2. Бета-плиссе:
Бета-плиссе:
β означает второе, и структура, описанная ниже, была вторым открытием после α-спирали.
Отличительные особенности этой конструкции:
я. Здесь цепь не спиральная, а зигзагообразная.
ii. Расстояние между каждым витком равно 7 Å.
III. Полипептидные цепи расположены рядом в виде складок.
РЕКЛАМА:
ив. Между цепями существует межцепочечная водородная связь, и каждая пептидная группа участвует в водородной связи.
Цепи антипараллельны друг другу.
3. Обратный поворот:
Складывается в обратном направлении цепи.
Третичная структура белков :Спиральная форма полипептида сворачивается в сферическую, глобулярную, эллипсоидальную или другую конформацию, которая называется третичной структурой белков. Эта укладка необходима для биологической активности белков. например, ферменты, иммуноглобулины.
Третичная конформация поддерживается четырьмя типами связей:
РЕКЛАМА:
1. Водородные связи:
Водородные связи:
Образуется между водородом и электроотрицательным атомом, таким как кислород или азот, в группе «R» аминокислот.
2. Ионные взаимодействия:
Образуется из кислых (глутаминовая и аспарагиновая) и основных (аргинин, лизин или гистидин) аминокислот.
3. Дисульфидные связки:
Это прочная связь, образованная между сульфгидрильными группами двух цистеиновых аминокислот. Образовавшаяся в результате димерная структура известна как цистин (аминокислота, содержащаяся только в белках, а не в свободной форме).
4. Гидрофобные взаимодействия:
Группы «R» гидрофобных аминокислот объединяются вместе в центре вдали от воды, тем самым развивая силу притяжения между каждой группой «R» и силу отталкивания от воды, и эти взаимодействия известны как гидрофобные взаимодействия.
Четвертичная структура белков: Четвертичная структура представлена олигомерными белками.
Олигомерные белки:
Имеют две или более полипептидные цепи.
Четвертичная структура относится к типу расположения полипептидов в олигомерном белке. Эти полипептиды удерживаются вместе водородными связями, ионными связями или силами Вандер-Ваальса, например, гемоглобин имеет четыре полипептидные цепи, которые расположены определенным образом, что относится к четвертичной структуре гемоглобина.
Четвертичная структура гемоглобина описывает, что он состоит из четырех полипептидных цепей; два из которых α (α 1 и α 2 ), а два других — β (β 1 и β 2 ). Две альфа-цепи противоположны друг другу и примыкают к каждой β-цепи. Цепи α и цепи β связаны между собой солевыми мостиками.
Структурно-функциональная связь в белках:
Гемоглобин играет жизненно важную роль в транспорте кислорода от легких к периферическим тканям и транспорте углекислого газа из тканей в легкие.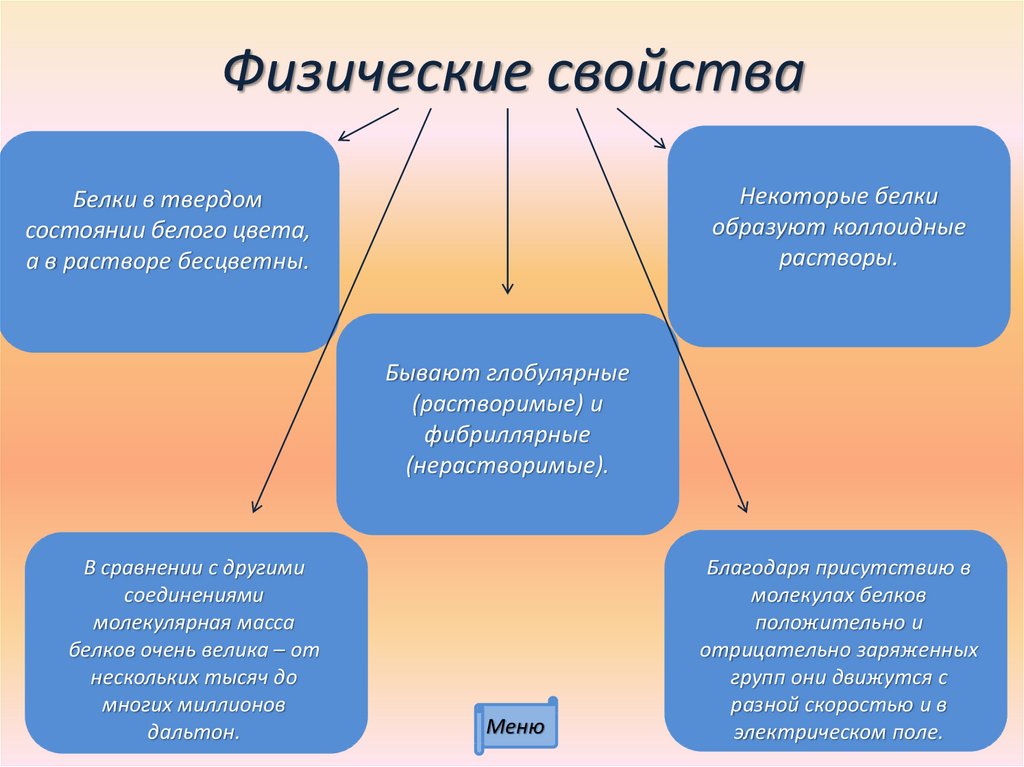
Существует три типа нормального гемоглобина со следующими полипептидами:
(1) Взрослый гемоглобин (Hb A) имеет цепи 2α2β.
(2) Фетальный гемоглобин (Hb F) имеет цепи 2α2γ.
(3) Малый взрослый гемоглобин (Hb A 1 ) имеет цепи 2α2δ.
Количество аминокислот в α-цепях составляет 141 аминокислоту, а в других цепях, то есть в β-, γ- и δ-цепях, 146 аминокислот. Эти цепи различаются по различию в последовательности расположения аминокислот в цепях. Четвертичная структура гемоглобина создает полость между тетрамером, в которой присутствует 2, 3, дифосфоглицерат (ДФГ или БФГ), образующий солевой мостик с амино-концом β-цепи, который стабилизирует гемоглобин, тем самым снижая сродство к кислороду.
В легких высокое парциальное давление кислорода приводит к связыванию O 2 с одной из цепей гемоглобина, разрывая тем самым солевые мостики между четырьмя субъединицами. Последующему связыванию кислорода (сигмовидная кривая ассоциации Hb-O 9 ) способствует разрыв солевых мостиков, изменяющий вторичную, третичную и четвертичную структуры, что позволяет вращать одну α/β-субъединицу по отношению к другой α/β-цепи, тем самым сжимая тетрамер и высвобождение ДФГ. Это приводит к увеличению его сродства к кислороду (состояние R Hb).
Это приводит к увеличению его сродства к кислороду (состояние R Hb).
В периферических тканях СО 2 связывается с а-аминогруппой аминоконца с преобразованием ее заряда из положительного в отрицательный, что способствует образованию солевого мостика между полипептидными цепями с возвратом в дезокси-состояние (Т-состояние), т. е. выделение кислорода из Hb. Высвобождению O 2 из Hb также способствует связывание DPG с тетрамером.
Когда человек взлетает в полет, аэроплан медленно набирает высоту, что приводит к снижению O 2 напряжение, из-за которого невозможна оксигенация гемоглобина. При этом человек испытывает гипоксию, но физиологический механизм организма начинает снижать выработку ДФГ, благодаря чему Hb может связывать кислород даже при более низком давлении кислорода.
Поэтому, когда аэроплан набирает максимальную высоту и держится стабильно, человек чувствует себя комфортно. Когда Hb достигает тканей, уровень ДФГ увеличивается, усиливая выделение кислорода. Точно так же вышеописанный процесс обращается вспять, когда человек ныряет глубоко в море. Высокий O 2 давление приводит к увеличению продукции ДФГ, что способствует оксигенации гемоглобина в легких и дезоксигенации в периферических тканях.
Точно так же вышеописанный процесс обращается вспять, когда человек ныряет глубоко в море. Высокий O 2 давление приводит к увеличению продукции ДФГ, что способствует оксигенации гемоглобина в легких и дезоксигенации в периферических тканях.
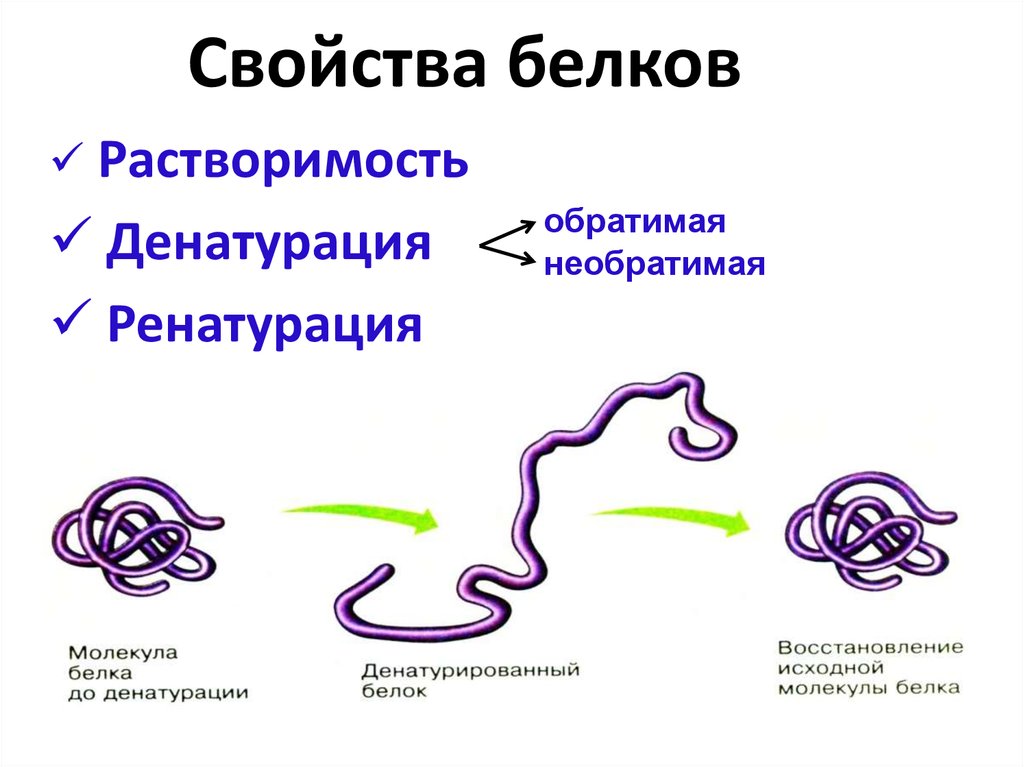
Частичное или полное разворачивание нативной (природной) конформации полипептидной цепи известно как денатурация. Это вызвано теплом, кислотами, щелочами, спиртом, ацетоном, мочевиной, бета-меркаптоэтанолом.
2. Коагуляция:Когда белки денатурируются нагреванием, они образуют нерастворимые агрегаты, известные как сгустки. Все белки не коагулируют при нагревании, лишь немногие, такие как альбумины и глобулины, способны коагулировать при нагревании.
3. Изоэлектрический pH (pH 1 ): рН, при котором белок имеет одинаковое количество положительных и отрицательных зарядов, называется изоэлектрическим рН. Под действием электрического поля белки не движутся ни к аноду, ни к катоду, поэтому это свойство используется для выделения белков. Белки становятся наименее растворимыми при pH 9.0404 I и попасть в осадок. pH I казеина составляет 4,5, и при этом pH казеин в молоке свертывается, образуя сгусток.
Под действием электрического поля белки не движутся ни к аноду, ни к катоду, поэтому это свойство используется для выделения белков. Белки становятся наименее растворимыми при pH 9.0404 I и попасть в осадок. pH I казеина составляет 4,5, и при этом pH казеин в молоке свертывается, образуя сгусток.
Средняя молекулярная масса аминокислоты принимается равной 110. Общее количество аминокислот в белке, умноженное на 110, дает приблизительную молекулярную массу этого белка. Разные белки имеют разный аминокислотный состав и, следовательно, их молекулярные массы различаются. Молекулярные массы белков колеблются от 5000 до 10 9 Дальтон. Экспериментально молекулярную массу можно определить такими методами, как гель-фильтрация, электрофорез в электрофорезе, ультрацентрифугирование или измерение вязкости.
Классификация белков :Белки классифицируются на основе:
(1) Их растворимость и
(2) Их структурная сложность.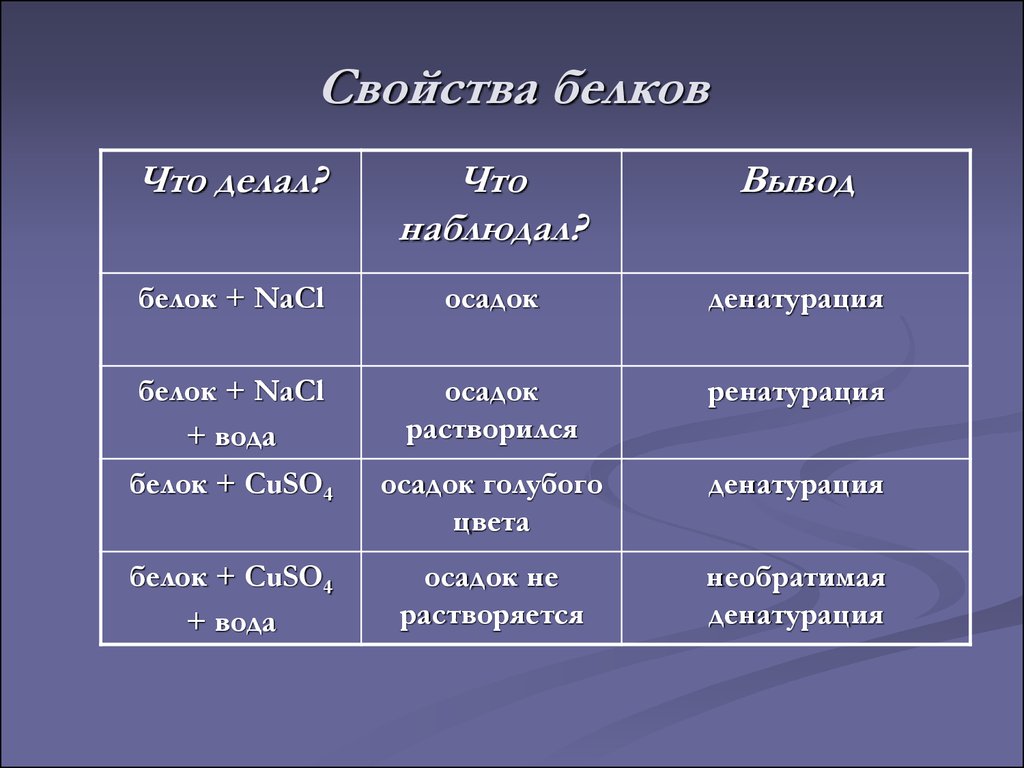
В зависимости от растворимости в воде белки подразделяются на:
1. Волокнистые белки:
Нерастворимы в воде. К ним относятся структурные белки. Они выполняют поддерживающую функцию (например, коллаген) и/или защитную функцию (например, кератин и фибрин волос).
2. Глобулярные белки:
Они растворимы в воде. К ним относятся функциональные белки, например ферменты, гемоглобин и т. д.
B. Классификация по сложности конструкции:В зависимости от сложности конструкции они подразделяются на:
(1) Простой
(2) конъюгированные и
(3) Производные белки.
1. Простые белки:
Белки, состоящие только из аминокислот, известны как простые белки.
Они далее подразделяются на:
(а) Альбумины:
Они растворимы в воде, коагулируют при нагревании и осаждаются при полном насыщении сульфатом аммония, например, сывороточный альбумин, лактальбумин и яичный альбумин.
(б) Глобулины:
Они нерастворимы в воде, но растворимы в разбавленных растворах солей. Они коагулируют при нагревании и осаждаются при половинном насыщении сульфатом аммония, например, сывороточный глобулин и овоглобулин.
(c) Глютелины:
Нерастворимы в воде и нейтральных растворителях. Растворим в разбавленных кислотах и щелочах. Они коагулируют под действием тепла, например глютелин пшеницы.
(г) Проламины:
Водонерастворимые, но растворимые в 70% спирте, например, глиадин пшеницы, белки кукурузы, ячменя и т. д.
(e) Истории:
Водорастворимый, основной по своей природе из-за присутствия аргинина и лизина, обнаруженный в ядре. Они помогают в упаковке ДНК в клетке. Они образуют белковую часть нуклеопротеина.
(f) Протамины:
Водорастворимый, основной по своей природе, не коагулируемый при нагревании. Найден в сперматозоидах, следовательно, является компонентом нуклеопротеина спермы.
(г) Глобины:
Они растворимы в воде, не коагулируют при нагревании. например, глобин гемоглобина.
(h) Альбуминоиды или склеропротеины:
Нерастворим во всех нейтральных растворителях, разбавленных кислотах или щелочах, например, кератин волос и белки костей и хрящей.
2. Конъюгированные белки:
Белки, состоящие из аминокислот и неаминокислотного/белкового вещества, называемого простетической группой, известны как конъюгированные белки.
Различные типы конъюгированных белков:
РЕКЛАМА:
(а) Хромопротеины:
Здесь небелковая часть представляет собой окрашенное соединение в дополнение к белковой части. Бывший. Гемоглобин имеет гем в качестве простетической группы, а цитохромы также имеют гем.
(б) Нуклеопротеины:
Эти белки связаны с нуклеиновыми кислотами, например, хроматином (гистоны + нуклеиновые кислоты).



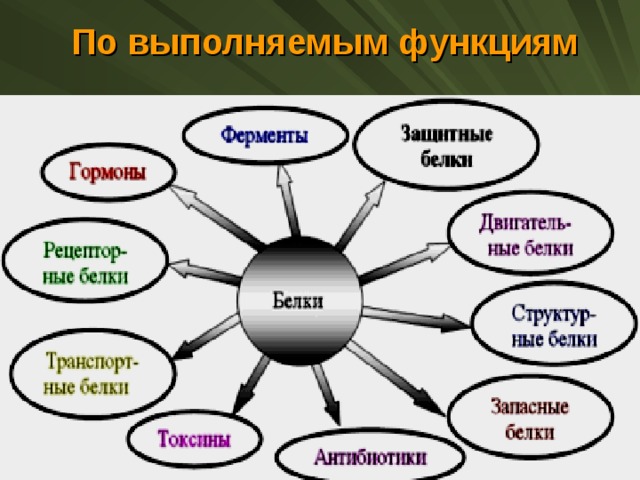

 Учащимся предоставлены ноутбуки. Просмотр видеоматериала с образовательного ресурса twig-bilim.kz. «Основы питания: Белки».
Учащимся предоставлены ноутбуки. Просмотр видеоматериала с образовательного ресурса twig-bilim.kz. «Основы питания: Белки». Строительными материалами белков являются:
Строительными материалами белков являются:
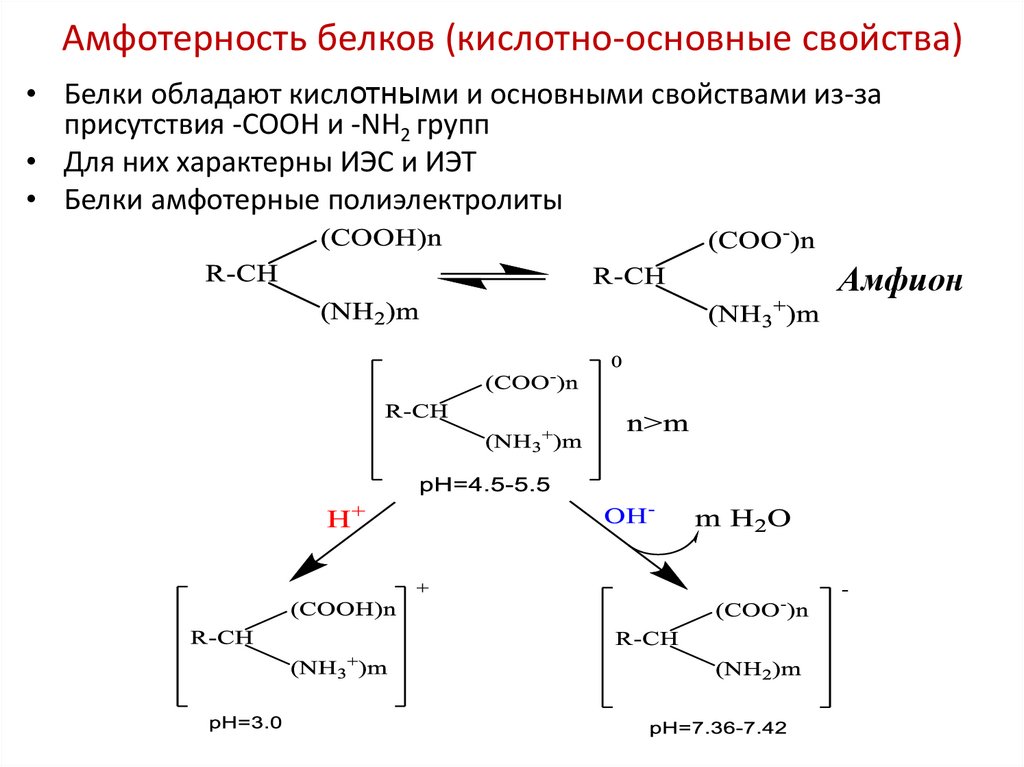
 Раздать листы с названиями и структурными формулами 20 аминокислот.
Раздать листы с названиями и структурными формулами 20 аминокислот.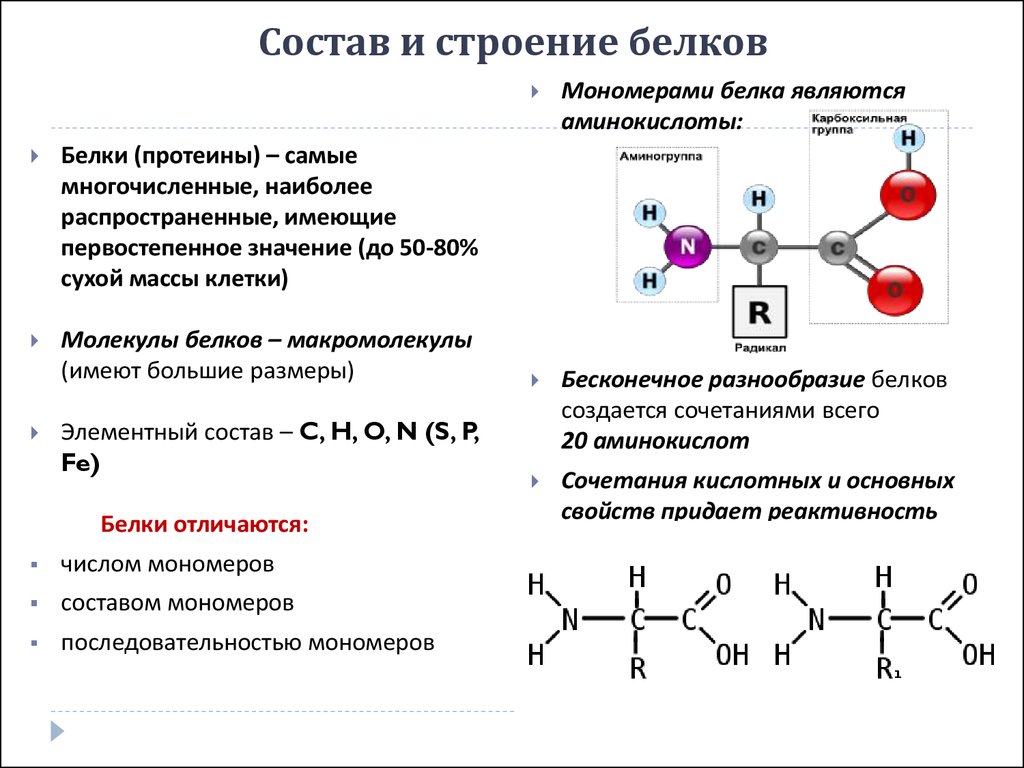 И чем больше мы устанавливаем связь между понятиями и образами, тем легче и быстрее они запоминаются.
И чем больше мы устанавливаем связь между понятиями и образами, тем легче и быстрее они запоминаются. kz/ru/courses/chemistry-ru/organicheskaya-ximiya/azotsoderzhashie-organicheskie-soedineniya/lesson/belki «Раздел Белки. Белки в нашем рационе питания»
kz/ru/courses/chemistry-ru/organicheskaya-ximiya/azotsoderzhashie-organicheskie-soedineniya/lesson/belki «Раздел Белки. Белки в нашем рационе питания»
 Предоставлены рабочие листы с ходом работы.
Предоставлены рабочие листы с ходом работы. Запишите наблюдения.
Запишите наблюдения.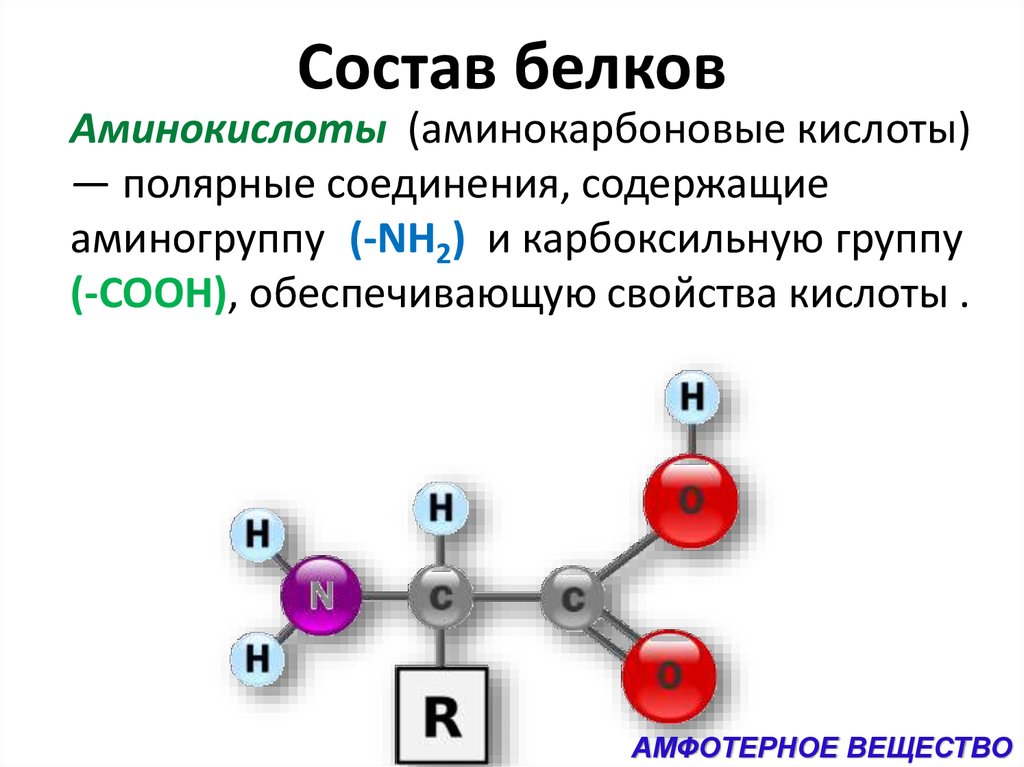
 kz/ru/courses/chemistry-ru/organicheskaya-ximiya/azotsoderzhashie-organicheskie-soedineniya/lesson/aminokisloty «Раздел: Аминокислоты»
kz/ru/courses/chemistry-ru/organicheskaya-ximiya/azotsoderzhashie-organicheskie-soedineniya/lesson/aminokisloty «Раздел: Аминокислоты»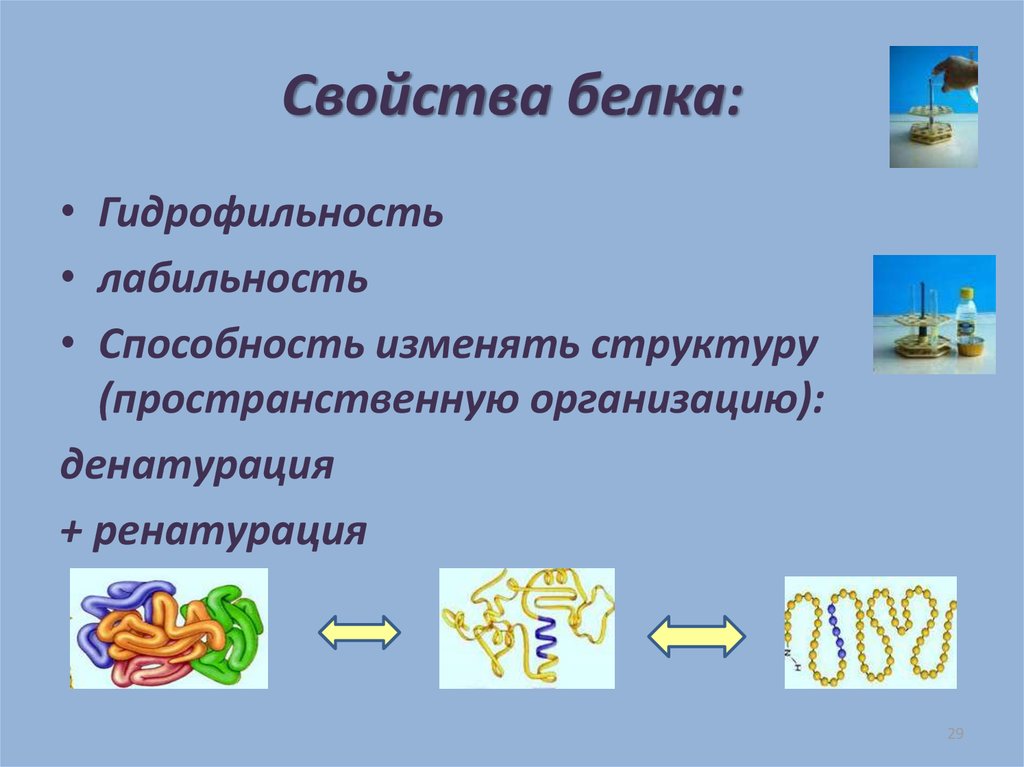 kz. «Раздел Тестовые вопросы», подраздел «Расчетные задачи по теме Углеводороды»
kz. «Раздел Тестовые вопросы», подраздел «Расчетные задачи по теме Углеводороды» Большинство исследований структуры белка было проведено с использованием этих белков. например, фибриноген, миозин и т. д.
Большинство исследований структуры белка было проведено с использованием этих белков. например, фибриноген, миозин и т. д. е. действуют как кислоты и щелочи. Они мигрируют в электрическом поле, и направление миграции зависит от суммарного заряда, которым обладает молекула. На чистый заряд влияет значение pH. Каждый белок имеет фиксированное значение изоэлектрической точки (pl), при которой он будет двигаться в электрическом поле.
е. действуют как кислоты и щелочи. Они мигрируют в электрическом поле, и направление миграции зависит от суммарного заряда, которым обладает молекула. На чистый заряд влияет значение pH. Каждый белок имеет фиксированное значение изоэлектрической точки (pl), при которой он будет двигаться в электрическом поле. е. являются левораторными.
е. являются левораторными.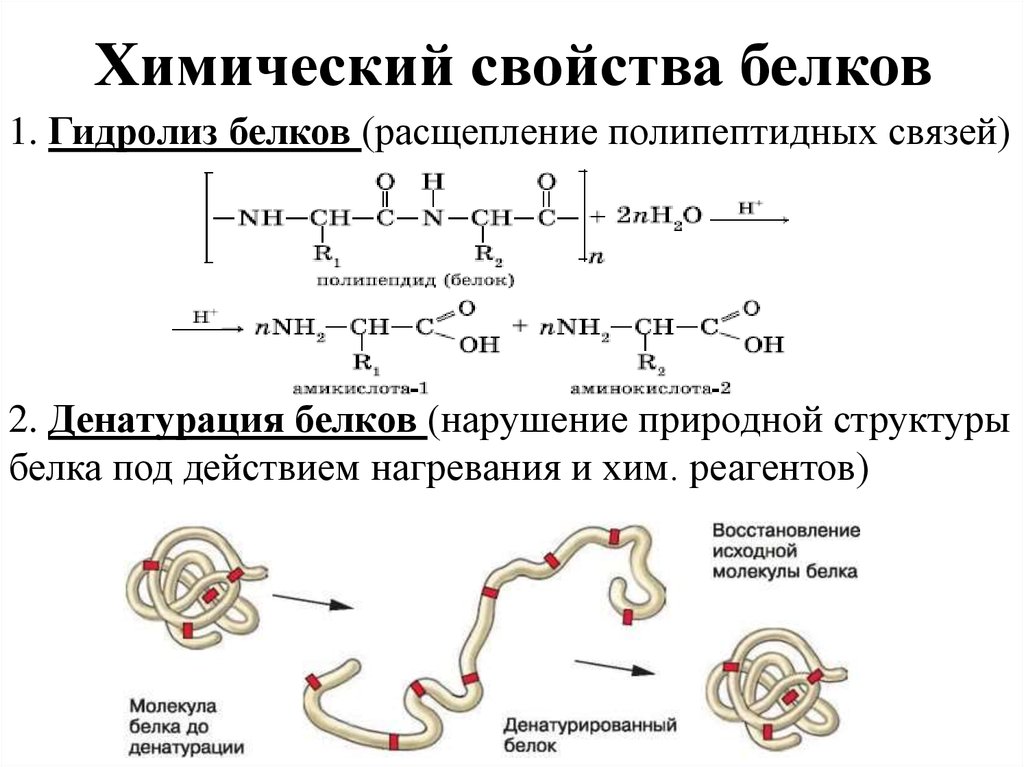 Реакция с азотистой кислотой (реакция Ван Слайка): Аминокислоты реагируют с HNO2 с выделением газообразного N2 и образованием соответствующих α-гидроксикислот.
Реакция с азотистой кислотой (реакция Ван Слайка): Аминокислоты реагируют с HNO2 с выделением газообразного N2 и образованием соответствующих α-гидроксикислот.  Реакция Паули
Реакция Паули